
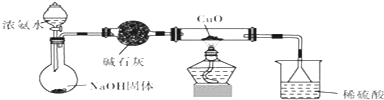
分析 【实验方案】
(1)要证明Cu(OH)2具有两性,应先加入碱生成Cu(OH)2,根据提供的药品可确定还需要的药品;
(2)根据质量守恒计算中含有1molCu,质量为64g,剩余为O元素;依据反应现象书写离子方程式;
(3)根据反应遵循质量守恒定律和该气体物污染确定气体的化学式;
【实验结论】
(4)根据两性氢氧化物的性质来分析,如具有两性,Cu(OH)2既能溶解于强酸,又能溶解于强碱;
(5)根据在不同温度下反应物的组成可确定物质的稳定性;
【问题讨论】
(6)A为Cu2O,在酸性条件下不稳定,可加入酸进行检验.
解答 解:【实验方案】(1)Cu不如Al活泼,可以用硫酸溶液进行验证,要证明Cu(OH)2具有两性,应先加入碱生成Cu(OH)2,药品中缺少氢氧化钠溶液,
故答案为:稀硫酸、氢氧化钠溶液;
(2)98g Cu(OH)2固体的物质的量为1mol,解热分解生成的72g固体中含有Cu的质量为1mol,即64g,则氧原子的质量为72g-64g8g,n(O)=$\frac{8g}{16g/mol}$=0.5mol,
则A中n(Cu):n(O)=2:1,向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在,说明生成了铜和铜离子,反应的离子方程式为:Cu2O+2H+=Cu+Cu2++H2O,
故答案为:Cu2O;Cu2O+2H+=Cu+Cu2++H2O;
(3)氧化铜和氨气反应生成红色物质铜,根据反应遵循质量守恒定律和该气体无污染确定气体为氮气,故答案为:N2;
【实验结论】
(4)如具有两性,Cu(OH)2既能溶解于强酸,又能溶解于强碱,分别生成盐和水,
故答案为:Cu(OH)2既能溶解于强酸,又能溶解于强碱;
(5)80℃~100℃时,得到黑色固体粉末,为CuO,继续加热到1000℃以上,黑色粉末全部变成红色粉末,说明在较高温度时Cu2O稳定,与酸反应生成硫酸铜和铜,说明在酸性条件下+2价的铜稳定,
故答案为:Cu+稳定性大于Cu2+;Cu2+稳定性大于Cu+;
【问题讨论】
(6)如含有Cu2O,根据其与酸反应的现象可判断,方程式为:Cu2O+H2SO4═Cu+CuSO4+H2O,溶液变蓝,而铜与稀硫酸不反应,取样加入稀硫酸,如果得到蓝色溶液和红色固体说明有A,如果不溶解说明无A,
故答案为:取NH3与CuO反应后生成的红色物质少许,加入稀硫酸中,若溶液变为蓝色,说明红色物质中含有A,反之则无.
点评 本题考查实验探究和数据处理,做题时注意两性氢氧化物的性质以及质量守恒定律计算物质的化学式,注意知识积累和熟练掌握,题目难度中等.


 小学教材全测系列答案
小学教材全测系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y的氧化物均能和水反应 | |
| B. | X与Y形成的化合物可能是离子化合物,也可能是共价化合物 | |
| C. | X的原子半径一定大于Y的原子半径 | |
| D. | X与Y的简单离子不可能具有相同的电子层结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2既可以是含硫物质的氧化产物,又可以是含硫物质的还原产物 | |
| B. | SO2是硫在空气中不完全燃烧的产物,SO3是硫在空气中完全燃烧的产物 | |
| C. | 大气中SO2的主要来源是汽车排出的尾气 | |
| D. | SO2具有漂白性,因而可以使石蕊试液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 部分难溶物的颜色和常温下的Ksp如下表所示:
部分难溶物的颜色和常温下的Ksp如下表所示:| Cu(OH)2 | CuOH | CuCl | Cu2O | |
| 颜色 | 蓝色 | 黄色 | 白色 | 砖红色 |
| Ksp(25℃) | 1.6×10-19 | 1.0×10-14 | 1.2×10-6 | - |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
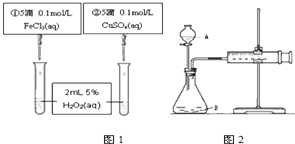
| A. | 图1实验可通过观察产生气泡快慢来比较反应速率的大小 | |
| B. | 若图1所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好 | |
| C. | 用图2装置可测定反应产生的气体体积 | |
| D. | 为检查图2装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为防止铁生锈,在其表面涂一层防锈油漆 | |
| B. | 为防止火灾,在面粉厂、加油站等场所要严禁烟火 | |
| C. | 为加快H2O2的分解速率,把反应容器放到冷水中冷却 | |
| D. | 为加快KClO3的分解速率,加入MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.10mol•L-1NH4HCO3溶液中通入CO2:c(NH4+)=c(HCO3-)+c(CO32-) | |
| B. | 0.10mol•L-1CH3COONa溶液中通入HCl:c(Na+)>c(Cl-)>c(CH3COOH) | |
| C. | 0.10mol•L-1Na2SO3溶液通入SO2:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)] | |
| D. | 向0.10mol•L-1NaHSO3溶液中通入NH3:c(Na+)>c(SO32-)>c(NH4+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 对氯苯甲酸是一种药物中间体,可用对氯甲苯为原料,通过高锰酸钾氧化法制备.反应如下:
对氯苯甲酸是一种药物中间体,可用对氯甲苯为原料,通过高锰酸钾氧化法制备.反应如下: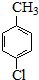 $→_{催化剂}^{KMnO_{4}}$
$→_{催化剂}^{KMnO_{4}}$
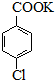 $\stackrel{H+}{→}$
$\stackrel{H+}{→}$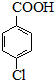
| 熔点/℃ | 沸点/℃ | 密度/g•cmˉ3 | 颜色 | 水溶性 | |
| 对氯甲苯 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
| 对氯苯甲酸 | 243 | 275 | 1.54 | 白色 | 微溶 |
| 对氯苯甲酸钾 | 具有盐的通性,属于可溶性盐,溶解度随温度升高而增大 | ||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com