
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:| 滴定次数 | 待测液体(mL) | 标准盐酸体积(mL) | |
| 滴定前读(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |
| 第三次 | 25.00 | 0.80 | 23.10 |
分析 (1)根据滴定终点,锥形瓶中的溶液颜色发生变化,且半分钟内不褪色;
(2)根据滴定时眼睛应观察锥形瓶内溶液颜色的变化;
(3)根据待测溶液润洗锥形瓶,会使的待测液的物质的量增多;根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析误差;
(4)根据酸式滴定管用蒸馏水洗净后,应用标准液润洗;
(5)根据滴定管的精确度为0.01mL读数;
(6)先根据数据分析舍去误差太大的数据,再根据c(待测)=$\frac{C(标准)×V(标准)}{V(待测)}$计算出c(待测);
(7)根据c(待测)=$\frac{C(标准)×V(标准)}{V(待测)}$分析误差;
解答 解:(1)用盐酸滴定氢氧化钠溶液以酚酞作指示剂,终点现象是当最后一滴标准液滴下,锥形瓶中溶液的颜色由红变无色,半分钟内颜色不再变化;
故答案为:当最后一滴标准液滴下,锥形瓶中溶液的颜色由红变无色,半分钟内颜色不再变化;
(2)滴定时边滴边摇动锥形瓶,眼睛应观察锥形瓶中颜色变化,以判定终点;
故答案为:锥形瓶内溶液颜色的变化;
(3)根据待测溶液润洗锥形瓶,会使的待测液的物质的量增多,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$,可知c(标准)偏大;
故答案为:待测溶液润洗锥形瓶;偏高;
(4)根据酸式滴定管用蒸馏水洗净后,应用标准液润洗;
故答案为:用盐酸标准液润洗酸式滴定管;
(5)滴定管中的液面读数为27.20mL;
故答案为:27.20;
(6)三次消耗盐酸的体积依次为:19.90mL、20.10mL、22.30mL,第3次误差较大,故取前两次的平均值:V(HCl)=20.00 mL,根据c(NaOH)=$\frac{0.1mol/L×20.00mL}{25.00mL}$=0.0800mol/L;
故答案为:0.0800;
(7)A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液,标准液浓度偏小,会导致测定标准液体积偏高,测定值偏高,故A错误;
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥,对标准液体积无影响,测定值不变,故B错误;
C.酸式滴定管在滴定前有气泡,滴定后气泡消失,会导致测定标准液体积偏大,测定值偏高,故C错误;
D.读取盐酸体积时,滴定结束时俯视读数,会导致测定标准液体积偏小,测定值偏低,故D正确;
故答案为:D.
点评 本题主要考查了中和滴定操作、误差分析以及计算,难度不大,理解中和滴定的原理是解题关键.


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇 | |
| B. | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | |
| C. | 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸 | |
| D. | 由氯代环己烷消去制环己烯;由丙烯加溴制1,2二溴丙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 双氧水被称为绿色氧化剂,是因为其还原产物为O2,对环境无污染 | |
| B. | 王水是浓盐酸和浓硝酸按体积比1:3配成的混合物,可溶解Au、Pt | |
| C. | 氨水能导电,说明氨气是电解质 | |
| D. | 往新制备的氯水中和SO2的水溶液中分别滴入石蕊试液时的现象不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 5 | C. | 7 | D. | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
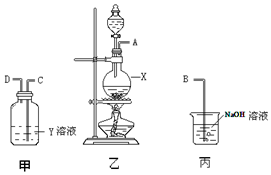 某化学课外兴趣小组为探究铜与浓硫酸反应气体产物的性质,拟用图所示的装置的组合进行实验.
某化学课外兴趣小组为探究铜与浓硫酸反应气体产物的性质,拟用图所示的装置的组合进行实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | ||||||
| D | E | F | |||||
| C | G | H |
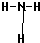 ,F的氢化物比同主族相邻元素的氢化物的沸点高,其原因是H2O分子间存在氢键.
,F的氢化物比同主族相邻元素的氢化物的沸点高,其原因是H2O分子间存在氢键.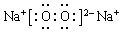 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | |
| B. | CH3COOCH2CH2OOCCH3 乙二酸二乙酯 | |
| C. | CH3CH2CH(OH)CH3 3-丁醇 | |
| D. | 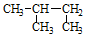 2-甲基丁烷 2-甲基丁烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com