
����Ŀ��ijͬѧ������������ȡ������������Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3 �� �������������ʣ���ȡ�̷���FeSO47H2O����������������̣�����˵������ȷ���ǣ� ��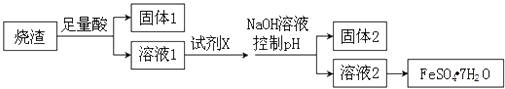
A.�ܽ�����ѡ���������ᣬ�Լ�Xѡ������
B.����1��һ������SiO2 �� ����pH��Ϊ��ʹAl3+ת��ΪAl��OH��3 �� �������2
C.���ı䷽��������Һ1��ֱ�Ӽ�NaOH���������õ��ij����������ܽ⣬����Һ���ᾧ����Ҳ�ɵõ�FeSO47H2O
D.����Һ2�õ�FeSO47H2O��Ʒ�Ĺ����У������������ֹ�������ͷֽ�
���𰸡�C
���������⣺��������ȡ������������Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3 �� �������������ʣ���������м����������ᣬFe2O3��Al2O3���ᷴӦ���ɵ������������������������費��Ӧ�����ˣ�����1Ϊ�������裻����Һ�м������۽������ӻ�ԭΪ�������ӣ�����pHֵʹ��������ȫ���������������������ˣ�����2Ϊ������������Һ2Ϊ��������������Ũ������ȴ�ᾧ�����ˣ��õ������������壬
A�������̷�����֪���ܽ�����ѡ���������ᣬXΪ���ۣ���A��ȷ��
B�������̷�����֪������1��һ������SiO2 �� ����pHֵʹ��������ȫ�����������������������2Ϊ������������B��ȷ��
C������Һ1�к��������Ӻ������ӣ��ӹ������������ƣ�������ת��Ϊƫ��������ӣ������������������ӽ���������������������������յõ�����������������������������C����
D�����������ױ������е���������������������ʧȥ�ᾧˮ�����Դ���Һ2�õ�FeSO47H2O��Ʒ�Ĺ����У������������ֹ�������ͷֽ⣬��D��ȷ��
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NaOH��AlCl3��MgCl2���ֹ�����ɵĻ�����������ˮ�к���0.58g��ɫ�������ɣ������õĻ���Һ�У���μ���0.5mol/L���ᣬ������������(V)�����ɳ���������(W)��ϵ����ͼ��ʾ��
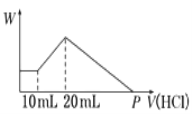
��1���������NaOH������Ϊ_________________
��2���������MgCl2������Ϊ_________________
��3���������AlCl3�����ʵ���Ϊ_________________
��4��P���ʾ����������_________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij���������к���NaCl���ʣ�Ϊ�ⶨ�����еĴ��������������������ͼ�е�װ�ý���ʵ�顣
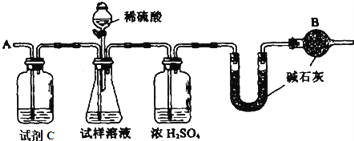
��Ҫʵ�鲽�����£�
�ٰ�ͼ��װ�����������װ�õ�������
�ڽ�a g����������ƿ�У�����������ˮ�ܽ⣬�õ�������Һ
�۳���ʢ�м�ʯ�ҵ�U�ܵ��������õ�b g
�ܴӷ�Һ©������6 mol��L-1�����ᣬֱ�����ٲ�������Ϊֹ
�ݴӵ���A����������һ�����Ŀ���
���ٴγ���ʢ�м�ʯ�ҵ�U�ܵ��������õ�c g
���ظ�����ݺ͢IJ�����ֱ��U�ܵ������������䣬Ϊd g
����պͻش����⣺
��1������������ƽ������Ʒʱ�������ƽ��ָ������ƫת��˵��___________��
��2��װ���и����B��������_______________��
��3���������Һ©���е����ỻ��Ũ����ͬ�����ᣬ���ԵĽ��___________����ƫ�ߡ�ƫ�ͻ䣩��
��4������ݵ�Ŀ����________________����5������ߵ�Ŀ����________________��
��5���������д�������������ļ���ʽΪ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���Ͷ�����˽����������������̣��������̲صķḻ��Դͨ���ܵ����͵�����������������ָ��������������Ҫ�ɷ���
A. CH4B. COC. H2 D. NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ�������ݻ���ͬ�������٢ڢ��н������·�Ӧ��3A��g��+B��g��2C��g����H��0������ʼ�¶���ͬ���ֱ�������������ͨ��3mol A��1mol B����ﵽƽ��ʱ��������C���ʵ���������ɴ�С��˳��Ϊ�� �� 
A.�ۢڢ�
B.�ۢ٢�
C.�٢ڢ�
D.�ڢ٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�1molX��n mol Y���ݻ�Ϊ2L���ܱ������з������·�Ӧ��X��g��+Y��g��2Z��g��+M��s����5min��ﵽƽ�⣬��ʱ����0.2mol Z������˵����ȷ���ǣ� ��
A.��������ѹ��ʱ�����淴Ӧ���ʾ�����
B.5 min��ƽ����Ӧ����v��X��=0.02 mol/��Lmin��
C.��ƽ������ϵ�м���l molM��s����ƽ�����淴Ӧ�����ƶ�
D.�����������������ٷ����仯ʱ��˵����Ӧ�ﵽƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Կ�����þΪԭ���Ʊ� Mg3N2 ��װ����ͼ��ʾ���гֺͼ���װ����ȥ����
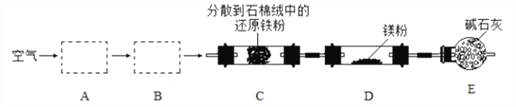
����˵����ȷ����
A. װ�� A��B �п����μ���Ũ���ᡢNaOH ��Һ
B. װ�� E �м�ʯ�ҵ�����������β��
C. ʵ��ʱ�� Ӧ�ȼ��� C��ͨ��һ��ʱ��������ټ���D
D. ��ȥ��װ�� C���Բ�Ʒ������Ӱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����8.12�����۱�ը����һ�������軯��й¶���軯�����������ˮ���о綾�������ˮ��Ⱦ��Ϊ�����Ӷ��軯����˽⣬ͬѧ�Dz������Ͻ���ѧϰ��̽���� 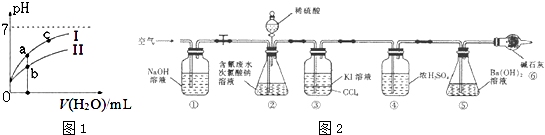
̽��һ��̽���軯�������
��֪��������ĵ���ƽ�ⳣ�����±���
���� | HCOOH | HCN | H2CO3 |
����ƽ�ⳣ�� | Ki=1.77��10��4 | Ki=5.0��10��10 | Ki1=4.3��10��7 |
��1��NaCN��Һ�ʼ��Ե�ԭ�����������ӷ���ʽ��ʾ��
��2����ͼ1��ʾ�����£�ϡ��HCOOH��HCN�������ϡ��Һʱ����ҺpH���ˮ���ı仯������˵����ȷ����
A.��ͬŨ�ȵ�HCOONa��NaCN�Ļ����Һ�У�������Ũ��
�Ĵ�С��ϵ�ǣ�c��Na+����c��CN������c��HCOO������c��OH������c��H+��
B.��NaCN��Һ��ͨ������������̼�����ӷ���ʽΪ��
CN��+CO2+H2O=HCN+CO32��
C.ͼ����a��c���㴦����Һ�� ![]() ��ȣ�HR����HCOOH��HCN��
��ȣ�HR����HCOOH��HCN��
D.ͼ����a�������Ũ��С��b�������Ũ��
��3��H2O2�С���ɫ�������������ƣ�Ҳ������ˮ�е��軯���KCN���������·�Ӧʵ�֣�KCN+H2O2+H2O�TA+NH3������������A�Ļ�ѧʽΪ ��
��4��̽�������ⶨ����ˮ���д����ٷ���
Ϊ�˲ⶨ����ˮ���д����ٷ��ʣ�ͬѧ��������ͼ2��ʾװ�ý���ʵ�飮��CN����Ũ��Ϊ0.2000mol/L�ĺ����ˮ100mL��100mL NaClO��Һ������������װ�â���ƿ�г�ַ�Ӧ����Һ©������������100mLϡH2SO4 �� �رջ�����
��֪װ�â��з�������Ҫ��Ӧ����Ϊ��
CN��+ClO���TCNO��+Cl��
2CNO��+2H++3C1O���TN2��+2CO2��+3C1��+H2O
������CN����ˮʱ������NaOH��Һ����pH��9ʱ����ʱc��CN����c��HCN�������������������=����
��5���ٺ͢������� ��
��6����Ӧ��������ͨ�˿�����Ŀ���� ��
��7��Ϊ�˼����ʵ��װ�â���ƿ�к����ˮ�������İٷ��ʣ�ʵ������Ҫ�ⶨװ����Ӧǰ�����������װ�âٵ�����ѡ����װ����ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н���������;������ķ�Ӧ����ʽ��ȷ���ǣ� ��
A.������������γɻ��漰��Ӧ��2H2SO3+O2 ![]() 2H2SO4
2H2SO4
B.��ҵ����ȡ�ֹ�Ļ�ѧ����ʽ��SiO2+C ![]() Si+CO2��
Si+CO2��
C.Na2 S203��Һ�м���ϡ���S2O+2H ![]() �TSO2+S��+HO2
�TSO2+S��+HO2
D.�ɷ�Ϊ����Ľ������84����Һ���ʹ�����ж���Cl��+ClO��+2H+�TCl2��+H20
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com