
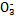 >Fe3+>I2,3Br2+6FeCl2
>Fe3+>I2,3Br2+6FeCl2 2FeBr3+4FeCl3;I2+2S2
2FeBr3+4FeCl3;I2+2S2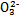
 S4
S4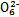 +2I-;CuIЪЧвЛжжАзЩЋГСЕэ(Ksp=1.3ЁС1
+2I-;CuIЪЧвЛжжАзЩЋГСЕэ(Ksp=1.3ЁС1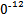 )ЁЃ
)ЁЃ| ЪЕбщВНжш | ЪЕбщЙ§ГЬКЭЯжЯѓ | ЖдгІНсТл | |
| ВНжш1 | ШЁвЛЖЈСПЕтбЮ,гУЪЪСПеєСѓЫЎШмНт,ВЂМгЯЁбЮЫсЫсЛЏ,НЋЫљЕУЪдвКЗжЮЊ3Зн | _____________ | |
| ВН жш 2 | ЕкЂйЗн ЪдвК | 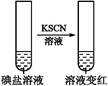 | ЕтбЮжаПЯЖЈКЌЁЁЁЁЁЁЁЁ |
| ЕкЂкЗн ЪдвК | 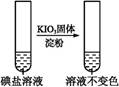 | _____________ | |
| ЕкЂлЗн ЪдвК | 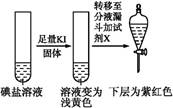 | XЮЊЁЁЁЁЁЁ(ЬюЛЏбЇЪН) | |
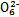 ЁЂI2ЁЂBr2ЕФбѕЛЏадгЩЧПЕНШѕЕФЫГађЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЂI2ЁЂBr2ЕФбѕЛЏадгЩЧПЕНШѕЕФЫГађЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ 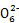
 2Fe2++I2,I
2Fe2++I2,I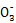 +5I-+6H+
+5I-+6H+ 3I2+3H2O
3I2+3H2O 2CuIЁ§+I2+4KCl
2CuIЁ§+I2+4KCl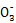 ОљгыI-ЗДгІ;Ђђ.вРОн2CuCl2+4KI
ОљгыI-ЗДгІ;Ђђ.вРОн2CuCl2+4KI 2CuIЁ§+I2+4KClЁЂI2+2S2
2CuIЁ§+I2+4KClЁЂI2+2S2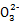
 S4
S4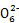 +2I-ПЩжЊCuCl2~S2
+2I-ПЩжЊCuCl2~S2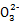 ,n(CuCl2)=n(S2
,n(CuCl2)=n(S2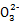 )=2ЁС10-3 mol,m(CuCl2ЁЄ2H2O)="0.342" g
)=2ЁС10-3 mol,m(CuCl2ЁЄ2H2O)="0.342" g


| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎNO2ЭЈШыAgNO3ШмвКжаЃК3NO2ЃЋH2OЃН2NO3ЃЃЋNOЃЋ2HЃЋ |
| BЃЎЙ§СПЕФSO2ЭЈШыNaOHШмвКжаЃКSO2ЃЋ2OHЃ=SO32-ЃЋH2O |
| CЃЎЙ§СПNaOHЕЮШыNH4HCO3ЯЁШмвКжаЃКNH4+ЃЋOHЃ=NH3ЁЄH2O |
| DЃЎЭЦЌМгШыЯЁHNO3жаЃКCuЃЋ2NO3ЃЃЋ4HЃЋ=Cu2ЃЋЃЋ2NO2ЁќЃЋ2H2O |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎKClO3ШмвК | BЃЎШлШкЕФNaCl | CЃЎKClОЇЬх | DЃЎТШЛЏЧтЦјЬх |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт

| AЃЎH+ЁЂMg2+ЁЂAl3+ | BЃЎMg2+ЁЂAl3+ЁЂFe2+ |
| CЃЎH+ЁЂBa2+ЁЂAl3+ | DЃЎжЛгаMg2+ЁЂAl3+ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎFe3+ | BЃЎFe2+ | CЃЎAl3+ | DЃЎNH4+ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎ0.8mol | BЃЎl mol | CЃЎ0.2mol | DЃЎ0.4mol |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
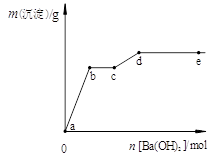
| AЃЎaЁњbЪБЕФГСЕэЕФГЩЗжЮЊBaSO4гыMg(OH)2 |
| BЃЎbЁњcЪБЗЂЩњЕФРызгЗДгІЮЊЃКH+ + OHЁЊ Ёњ H2O |
| CЃЎcЁњdЪБРызгЕФЮяжЪЕФСПЃКBa2+ПЩФмДѓгкClЁЊ |
| DЃЎdЁњeЪБРызгЕФЮяжЪЕФСПЃКBa2+вЛЖЈДѓгкOHЁЊ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт

| AЃЎМзЮЊAlCl3ЃЌввЮЊNaHCO3 |
| BЃЎШмвКБћжаЛЙПЩвдДѓСПЙВДцЕФРызггаЃКFe2+ЁЂNO3ЁЊЁЂSO42ЁЊ |
| CЃЎдкМзжаЕЮМгЖЁПЊЪМЗДгІЕФРызгЗНГЬЪНЃКHCO3ЁЊ+ Ba2++OHЁЊ= BaCO3Ё§+ H2OЁЃ |
| DЃЎАзЩЋГСЕэAПЩФмШмНтдкШмвКDжаЁЃ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЬюПеЬт
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com