
| A. | 0.08mol/L | B. | 0.0018mol/L | C. | 0.075mol/L | D. | 0.0075mol/L |
分析 Br2能氧化H2SO3,向含有HBr和H2SO3的溶液里通入氯气,氯气先和亚硫酸反应生成硫酸,然后氯气再和溴离子反应生成溴单质,根据氧化还原反应中得失电子守恒计算原溶液中H2SO3的浓度,进而计算SO42-的浓度.
解答 解:设亚硫酸和溴化氢的物质的量都为x.氯气和溴化氢、亚硫酸反应的方程式分别为:Cl2+2HBr=Br2+2HCl、Cl2+H2SO3+H2O=H2SO4+2HCl,
由方程式知,反应中氯元素得电子的物质的量为0.01mol×2=0.02mol;硫元素失电子的物质的量为x×(6-4)=2x,溴元素失电子的物质的量为x×1×$\frac{1}{2}$=0.5x,根据氧化还原反应中得失电子数相等得0.02mol=2x+0.5x,x=0.008mol,所以原溶液中HBr和H2SO3的浓度都为$\frac{0.008mol}{0.1L}$=0.08mol/L,亚硫酸完全转化为硫酸根离子,则反应后溶液中SO42-的浓度等于H2SO3的浓度,即为0.08mol/L.
故选A.
点评 本题考查了氧化还原反应的计算,难度不大,根据氧化还原反应中得失电子守恒进行分析解答即可.


 星级口算天天练系列答案
星级口算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 空气是一种宝贵的资源 | |
| B. | 空气中氮气的质量分数为78% | |
| C. | 氧气易溶于水,供给水生生物呼吸 | |
| D. | 汽车尾气随意排放,与雾霾形成无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 加入物质 | 碳酸钠溶液 | 氢氧化钡溶液 | 氧化铜粉末 |
| 现象 | 产生无色气体 | 产生白色沉淀 | 固体溶解 |
| A. | HCl | B. | CaCl2 | C. | MgSO4 | D. | H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
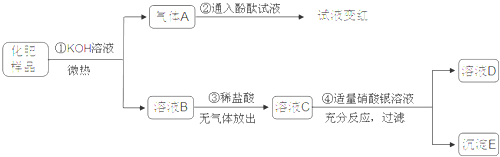
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一种离子对带异性电荷离子的吸引作用与其所处的方向无关,故离子键无方向性 | |
| B. | 因为离子键无方向性,故阴、阳离子的排列是没有规律的、随意的 | |
| C. | 因为氯化钠的化学式是NaCl,故每个Na+周围吸引一个Cl- | |
| D. | 因为离子键无饱和性,故一种离子周围可以吸引任意多个带异性电荷的离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
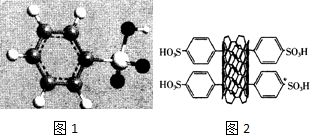 如图的分子结构模型A(相对分子质量为M)是由4种半径依次增大的短周期元素X、Y、Z、M构成,该物质溶于水显强酸性.请回答下列问题.
如图的分子结构模型A(相对分子质量为M)是由4种半径依次增大的短周期元素X、Y、Z、M构成,该物质溶于水显强酸性.请回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com