
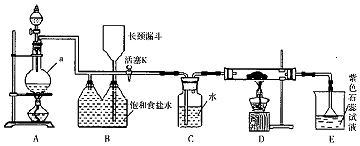
·ÖĪö £Ø1£©AÖŠ¶žŃõ»ÆĆĢÓėÅØŃĪĖįŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³ÉĀČĘų”¢ĀČ»ÆĆĢŗĶĖ®£»
£Ø2£©ŅĄ¾ŻŅĒĘ÷µÄŠĪדĖµ³öĘäĆū³Ę£»
£Ø3£©ŅĄ¾ŻĢāøɽįŗĻŌ×ÓøöŹżŹŲŗćæÉÖŖĀČĘųÓėĢ¼”¢Ė®ÕōĘų·“Ӧɜ³ÉĀČ»ÆĒāŗĶ¶žŃõ»ÆĢ¼£»ĀČ»ÆĒāĘųĢ弫Ņ×ČÜÓŚĖ®£¬ĒŅĖ®ÄÜĢį¹©Ė®ÕōĘų£¬¾Ż“Ė·ÖĪö£»
£Ø4£©ĀČĘųÓėĖ®·“Ӧɜ³ÉŃĪĖįŗĶ“ĪĀČĖį£¬ŃĪĖį¾ßÓŠĖįŠŌ£¬“ĪĀČĖį¾ßÓŠĘư׊Ō£¬¾Ż“ĖÅŠ¶ĻĻÖĻó£»
£Ø5£©ĀČ»ÆĒā”¢“ĪĀČĖįŗĶ³ĪĒåŹÆ»ŅĖ®·“Ó¦¶¼Éś³ÉæÉČÜŠŌµÄŃĪŗĶĖ®£»
£Ø6£©øł¾ŻB×°ÖĆÄŚĘųĢåµÄŃ¹Ēæ±ä»Æ·ÖĪöŅŗĆę±ä»Æ£»Čō·¢ĻÖ×°ÖĆBÖŠøĆĻÖĻó²»Ć÷ĻŌ£¬æÉÄÜŹĒA»ņB×°ÖĆĀ©Ęų£¬ĀČĘųŗĶ°±ĘųĻąÓö£¬ÓŠÅØŗńµÄ°×ŃĢ²¢ŌŚČŻĘ÷ÄŚ±ŚÄż½į£¬Ķ¬Ź±Éś³ÉŅ»ÖÖ³£¼ūµÄĘųĢåµ„ÖŹ£¬°×ŃĢĪŖĀČ»Æļ§”¢µ„ÖŹĪŖµŖĘų£®
½ā“š ½ā£ŗ£Ø1£©¶žŃõ»ÆĆĢÓėÅØŃĪĖįŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³ÉĀČĘų”¢ĀČ»ÆĆĢŗĶĖ®£¬»Æѧ·½³ĢŹ½£ŗMnO2+4HCl£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$MnCl2+Cl2”ü+2H2O£»
¹Ź“š°øĪŖ£ŗMnO2+4HCl£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$MnCl2+Cl2”ü+2H2O£»
£Ø2£©aŅĒĘ÷µÄĆū³ĘĪŖŌ²µ×ÉÕĘ棻
¹Ź“š°øĪŖ£ŗŌ²µ×ÉÕĘ棻
£Ø3£©ĀČĘųÓėĢ¼”¢Ė®ÕōĘų·“Ӧɜ³ÉĀČ»ÆĒāŗĶ¶žŃõ»ÆĢ¼£¬»Æѧ·½³ĢŹ½£ŗ2Cl2+C+2H2O$\frac{\underline{\;\;”÷\;\;}}{\;}$4HCl+CO2£»ŃĪĖįÓŠ»Ó·¢ŠŌ£¬ĖłŅŌÖĘČ”µÄĀČĘųÖŠŗ¬ÓŠĀČ»ÆĒāĘųĢ壬ĀČ»ÆĒā¼«Ņ×ČÜÓŚĖ®£¬ĶعżŅŌÉĻ·ÖĪöÖŖ£¬C×°ÖƵÄ×÷ÓĆŹĒ£ŗĪüŹÕCl2ÖŠµÄHClĘųĢ壬Ģį¹©D“¦ĖłŠčĖ®ÕōĘų£¬
¹Ź“š°øĪŖ£ŗ2Cl2+C+2H2O$\frac{\underline{\;\;”÷\;\;}}{\;}$4HCl+CO2£» ĪüŹÕHClĘųĢ壬²¢Ģį¹©Ė®ÕōĘų²ĪÓėDÖŠ·“Ó¦£»
£Ø4£©ĀČĘųÓėĖ®·“Ӧɜ³ÉŃĪĖįŗĶ“ĪĀČĖį£¬ŃĪĖį¾ßÓŠĖįŠŌÄܹ»Ź¹ŹÆČļČÜŅŗÓÉ×ĻÉ«±äĪŖŗģÉ«£¬“ĪĀČĖį¾ßÓŠĘư׊ŌÄܹ»Ź¹±äŗģµÄČÜŅŗĶŹÉ«£¬ĖłŅŌĻÖĻóĪŖ£ŗÓÉ×ĻÉ«±äĪŖŗģÉ«£¬ŌŁ±äĪŖĪŽÉ«£»
¹Ź“š°øĪŖ£ŗÓÉ×ĻÉ«±äĪŖŗģÉ«£¬ŌŁ±äĪŖĪŽÉ«£»
£Ø5£©Ź£ÓąµÄĀČĘųŌŚE×°ÖĆÖŠŗĶĖ®·“Ӧɜ³ÉŃĪĖįŗĶ“ĪĀČĖį£¬ĀČ»ÆĒā”¢“ĪĀČĖįŗĶ³ĪĒåŹÆ»ŅĖ®·“Ó¦¶¼Éś³ÉæÉČÜŠŌµÄŃĪŗĶĖ®£¬ĖłŅŌ·“Ó¦¹ż³ĢĪŽĻÖĻóĪŽ°×É«³ĮµķÉś³É£¬
¹Ź“š°øĪŖ£ŗ¢Ś£»
£Ø6£©D“¦·“Ó¦Ķź±Ļŗ󣬹Ų±ÕŠżČūK£¬ŅĘČ„¾Ę¾«µĘ£¬µ«ÓÉÓŚÓąČȵÄ×÷ÓĆ£¬A“¦ČŌÓŠCl2²śÉś£¬ĘųĢåĶعżµ¼¹Ü½ųČėB×°ÖĆ£¬µ¼ÖĀB×°ÖĆÖŠĘųĢåµÄŃ¹ĒæŌö“󣬓óÓŚ“óĘųŃ¹£¬ĘČŹ¹ĘæÖŠŅŗĆęĻĀ½µ£¬³¤¾±Ā©¶·ÄŚŅŗĆęÉĻÉż£¬Čō·¢ĻÖ×°ÖĆBÖŠøĆĻÖĻó²»Ć÷ĻŌ£¬æÉÄÜŹĒA»ņB×°ÖĆĀ©Ęų£¬ĀČĘųŗĶ°±ĘųĻąÓö£¬ÓŠÅØŗńµÄ°×ŃĢ£¬°×ŃĢĪŖĀČ»Æļ§Ķ¬Ź±Éś³Éµ„ÖŹĪŖµŖĘų£¬øĆ·“Ó¦ĪŖ3Cl2+8NH3ØT6NH4Cl+N2£¬
¹Ź“š°øĪŖ£ŗ×°ÖĆBÖŠĘæÄŚŅŗĆęĻĀ½µ£¬³¤¾±Ā©¶·ÄŚŅŗĆęÉĻÉż£»A»ņB×°ÖĆĀ©Ęų£»3Cl2+8NH3ØT6NH4Cl+N2£®
µćĘĄ ±¾ĢāĪŖŅŌĀČĘųµÄÖĘČ”ŗĶŠŌÖŹ½įŗĻµÄŹµŃéĢā£¬ŹģĻ¤ĀČĘųÖʱøµÄŌĄķ¼°ĀČĘų”¢ĀČĖ®µÄŠŌÖŹŹĒ½āĢā¹Ų¼ü£¬×¢Ņā½įŗĻĢāøÉŠÅĻ¢”¢Įé»īŌĖÓĆĪļÖŹÖ®¼äµÄ·“Ó¦£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 25”ę£¬1.01”Į105Pa£¬64 g SO2ÖŠŗ¬ÓŠµÄŌ×ÓŹżĪŖ3NA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬1.06 g Na2CO3ŗ¬ÓŠµÄNa+øöŹżĪŖ0.02NA | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬32 g O2ŗĶO3µÄ»ģŗĻĘųĢåĖłŗ¬Ō×ÓŹżĪŖ2NA | |
| D£® | ŗ¬ÓŠNAøöŃõŌ×ÓµÄŃõĘųŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ22.4 L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | øıäµÄĢõ¼ž | ½įĀŪ |
| A | ÉżĪĀ | CO32-µÄĖ®½āĘ½ŗāĻņÓŅŅĘ¶Æ |
| B | ¼ÓČėAlCl3¹ĢĢå | ²śÉś“óĮæĘųĢå |
| C | ¼ÓČė100mLH2O | ČÜŅŗÖŠc£ØH+£©”¢c£ØOH-£©¾ł¼õŠ” |
| D | ¼ÓČėÉŁĮæCH3COONa¹ĢĢå | ČÜŅŗÖŠn£ØCO32-£©Ōö“ó |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na0H¹ĢĢåŌŚæÕĘųÖŠ±äÖŹ | B£® | øÖĢśÉśŠā | ||
| C£® | ĪļÖŹµÄČ¼ÉÕ | D£® | Ö²ĪļµÄ¹āŗĻ×÷ÓĆ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
| a”¢bæÉÄܵĹŲĻµ | Éś³ÉµÄ³ĮµķµÄÖŹĮæ/g |
| bӆ3a | 2.6b |
| b”Ż4a | 0 |
| 3a£¼b£¼4a | 31.2a-7.8b |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
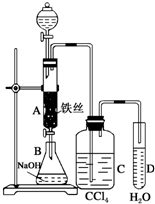 ij»ÆѧæĪĶāŠ”×éÓĆČēĶ¼ĖłŹ¾µÄ×°ÖĆÖĘČ”äå±½£®ĻČĻņ·ÖŅŗĀ©¶·ÖŠ¼ÓČė±½ŗĶŅŗä壬ŌŁ½«»ģŗĻŅŗĀżĀżµĪČė·“Ó¦Ę÷A£ØAĻĀ¶Ė»īČū¹Ų±Õ£©ÖŠ£®
ij»ÆѧæĪĶāŠ”×éÓĆČēĶ¼ĖłŹ¾µÄ×°ÖĆÖĘČ”äå±½£®ĻČĻņ·ÖŅŗĀ©¶·ÖŠ¼ÓČė±½ŗĶŅŗä壬ŌŁ½«»ģŗĻŅŗĀżĀżµĪČė·“Ó¦Ę÷A£ØAĻĀ¶Ė»īČū¹Ų±Õ£©ÖŠ£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com