
【题目】看图回答下列问题 
(1)若烧杯中溶液为稀硫酸,则观察到的现象是 , 电流表指针(填偏转或不偏转),两极反应式为:正极;负极 .
(2)若烧杯中溶液为氢氧化钠溶液,则负极为(填Mg或Al),总反应方程式为
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:A、B两个电极均由多孔的碳块组成.该电池的正极反应式为: .
(4)如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电 池装置,电池的总反应方程式为:CH4+2O2+2KOH=K2CO3+3H2O,则该电池的负极反应式为: .
【答案】
(1)镁逐渐溶解,铝极上有气泡冒出;偏转;2H++2e﹣=H2↑;Mg﹣2e﹣=Mg2+
(2)Al;2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(3)O2+2H2O+4e﹣=4OH﹣
(4)CH4+8e﹣+10OH﹣=CO32﹣+7H2O
【解析】解:(1.)镁、铝和稀硫酸构成了原电池,自发进行的反应是镁和硫酸反应,金属镁做负极,电极反应:Mg﹣2e﹣=Mg2+ , 金属铝为正极,溶液中的2H+得到电子发生还原反应,电极反应为:2H++2e﹣=H2↑,所以可看到镁逐渐溶解,铝极上有气泡冒出,电流表指针发生偏转,所以答案是:镁逐渐溶解,铝极上有气泡冒出;电流表指针发生偏转;Mg﹣2e﹣=Mg2+;2H++2e﹣=H2↑.
(2.)镁、铝和氢氧化钠溶液构成了原电池,自发的氧化还原反应是金属铝和氢氧化钠之间的反应,总反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,铝失电子,为负极,金属镁作正极,所以答案是:Al;2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(3.)氢气、氧气和氢氧化钾溶液构成了原电池,自发的氧化还原反应是氢气和氧气之间的反应,总反应方程式为:2H2+O2=2H2O,,正极上通的是氧气,B极是正极,电极反应:O2+2H2O+4e﹣=4OH﹣ , 所以答案是:O2+2H2O+4e﹣=4OH﹣
(4.)燃料电池的总反应离子方程式为:CH4+2O2+2OH﹣=CO32﹣+3H2O,正极上通的是氧气,电极反应:2O2+4H2O+8e﹣=8OH﹣ , 负的极一定是燃料失电子的过程,因正极和负极相加即为总反应,所以:CH4+8e﹣+10OH﹣=CO32﹣+7H2O,
所以答案是:CH4+8e﹣+10OH﹣=CO32﹣+7H2O.


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】某有机物的分子式为C5H10O,它能发生银镜反应和加成反应,若将它与H2加成,所得产物结构简式是( )
A.(CH3)2CCH2OH
B.(CH3CH2)2CHOH
C.CH3(CH2)3CH2OH
D.CH3CH2C(CH3)2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是表示物质组成、结构和变化规律的一种具有国际性、科学性和规范性的书面语言。下列化学用语中书写正确的是
A. 含有6个质子、8个中子的碳元素的核素符号:126C
B. N2的电子式: ![]()
C. O2-的结构示意图: ![]()
D. 氯化氢的电子式: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH溶被的体积和所得沉淀的物质的量的关系如图所示(b处NaOH溶液的体积为2L),则下列判断正确的是
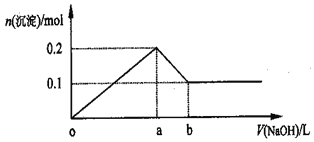
A. NaOH溶液的物质的量浓度为0.5mol/L
B. 混合溶液中A13+与Mg2+物质的量之比为2:1
C. a点时消耗NaOH溶液的体积与b点时消耗NaOH溶液的体积之比为5:1
D. 在b处溶液中的溶质只有Na[Al(OH)4]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于纯净物、混合物、电解质、非电解质的正确组合为( )
纯净物 | 混合物 | 电解质 | 非电解质 | |
A | 盐酸 | 水煤气 | 硫酸 | 干冰 |
B | 蒸馏水 | 蔗糖溶液 | 氯化氢 | 二氧化硫 |
C | 胆矾 | 盐酸 | 铁 | 碳酸钙 |
D | 胆矾 | 水煤气 | 氯化铜 | 碳酸钠 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列有机化学的认识中,错误的是
A. 反应 ![]() 属于取代反应
属于取代反应
B. 淀粉和纤维素属于多糖,在人体内水解转化为葡萄糖,为人类提供能量
C. 分枝酸结构简式如图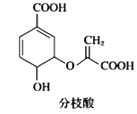 ,可与乙醇、乙酸反应,也可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色
,可与乙醇、乙酸反应,也可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色
D. 取蔗糖水解液少许,先滴加过量的NaOH溶液,再滴入新制的氢氧化铜悬浊液,加热,有红色沉淀生成,证明其水解产物具有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铁及其化合物的说法正确的是( )
A.将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红,可以检验Fe(NO3)2晶体是否已氧化变质
B.浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体
C.1 mol FeI2与足量氯气反应时转移的电子数为2NA
D.水溶液中Fe2+、H+、SO ![]() 、ClO﹣不能大量共存
、ClO﹣不能大量共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学常见单质A、B和甲、乙、丙三种化合物有如图所示的转换关系(部分产物未列出).单质A常作为食品包装材料,甲是两性氧化物. 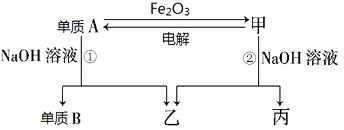
根据图示转化关系回答:
(1)写出下列物质的化学式:单质A , 乙 .
(2)写出单质A与Fe2O3反应的化学方程式: , 利用该反应的原理,可用于
(3)用单质A做成的容器可以储存和运输浓硫酸的原因是 .
(4)写出反应①的离子方程式: .
(5)工业上冶炼下列物质通常 不采用电解法的是 .
a.Na b.Mg c.Fe d.Ag
(6)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有
a.KCl b.KClO 3 c.MnO2 d.Mg.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com