
| A. | IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VIIA族元素氢化物沸点顺序也是:HBr>HCl>HF | |
| B. | CH4是正四面体结构,则SiH4也是正四面体结构 | |
| C. | 锂与氧气反应:4Li+O2$\frac{\underline{\;加热\;}}{\;}$2 Li2O,则钠与氧气反应:4Na+O2$\frac{\underline{\;加热\;}}{\;}$2Na2O | |
| D. | CaCO3与稀硝酸反应生成CO2,则CaSO3与稀硝酸反应生成SO2 |
分析 A.IVA族元素氢化物中相对分子质量越大,沸点越大;而VIIA族元素氢化物中HF分子间含氢键,沸点最高;
B.C、Si的最外层电子数均为4,且氢化物中均形成4个单键;
C.钠与氧气加热反应生成过氧化钠;
D.CaSO3与稀硝酸发生氧化还原反应.
解答 解:A.IVA族元素氢化物中相对分子质量越大,沸点越大,则沸点顺序是:GeH4>SiH4>CH4;而VIIA族元素氢化物中HF分子间含氢键,沸点最高,沸点为HF>HBr>HCl,类比不合理,故A错误;
B.C、Si的最外层电子数均为4,且氢化物中均形成4个单键,CH4是正四面体结构,则SiH4也是正四面体结构,类比合理,故B正确;
C.钠比Li活泼,锂与氧气发生4Li+O2$\frac{\underline{\;加热\;}}{\;}$2 Li2O,而钠与氧气发生2Na+O2$\frac{\underline{\;加热\;}}{\;}$Na2O2,类比不合理,故C错误;
D.CaCO3与稀硝酸发生复分解反应生成CO2,CaSO3与稀硝酸发生氧化还原反应生成硫酸钙、NO和水,类比不合理,故D错误;
故选B.
点评 本题考查类比法应用,为高频考点,把握物质的性质、发生的反应、反应规律为解答的关键,侧重分析与应用能力的考查,注意氢键、氧化还原反应的应用,题目难度不大.


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 大于0.2mol•L-1 | B. | 等于0.2mol•L-1 | C. | 小于0.2mol•L-1 | D. | 无法估算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
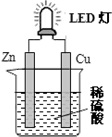
| A. | 锌片表面有气泡生成 | |
| B. | 装置中存在“化学能→电能→光能”的转换 | |
| C. | 如果将硫酸换成柠檬汁,导线中就不会有电子流动 | |
| D. | 如果将铜片换成锌片,LED灯仍然会发光 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
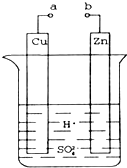 原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.
原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.
50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| ① | ||||||||
| ② | ③ | |||||||
| ④ | ⑤ | ⑥ | ||||||
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

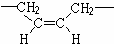 ,若顺丁橡胶的平均相对分子质量为540108,则平均聚合度为10002.
,若顺丁橡胶的平均相对分子质量为540108,则平均聚合度为10002.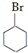 +NaOH$\stackrel{△}{→}$
+NaOH$\stackrel{△}{→}$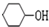 +NaBr.
+NaBr.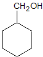 的合成路线.
的合成路线.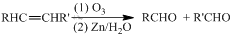 (R,R’代表烃基或氢)CH2=CHCH=CH2$\stackrel{催化剂}{→}$
(R,R’代表烃基或氢)CH2=CHCH=CH2$\stackrel{催化剂}{→}$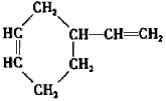

 $→_{催化剂}^{氢气}$
$→_{催化剂}^{氢气}$ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都能在空气中燃烧 | |
| B. | 都容易发生取代反应 | |
| C. | 苯和乙烯都能在一定条件下发生加成反应 | |
| D. | 苯不能使酸性KMnO4溶液褪色而乙烯能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W | ||
| T |
| A. | Y氢化物的沸点一定比X氢化物的沸点高 | |
| B. | Z的最高价氧化物的水化物酸性比W的强 | |
| C. | XZ2、XW4 与Na2O的化学键类型相同 | |
| D. | 根据元素周期律,可以推测存在TZ2和TW4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com