
【题目】由Zn、Cu、Al、Fe四种金属中的两种组成的混合物41.5g,与足量的盐酸反应产生的氢气在标况下为22.4升,则混合物中一定含有的金属是 ( )
A.ZnB.FeC.AlD.Cu
【答案】C
【解析】
把两种金属看成一种金属,且反应后显+2价,令金属为R,与盐酸反应:R+2HCl=RCl2+H2↑,根据量,求出R的摩尔质量,然后进行分析;
把两种金属看成一种金属,令该金属为R,反应后金属显+2价,令R的摩尔质量为ag·mol-1,R与盐酸反应: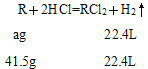 ,解得a=41.5。所以两种金属混合,要求金属折算成+2价后,一种金属的摩尔质量大于41.5g/mol,另一种小于41.5 g/mol,Zn的摩尔质量为65g·mol-1,Fe的摩尔质量为56g·mol-1,Al与盐酸反应后生成AlCl3,Al显+3价,转化成+2价,Al的摩尔质量为18g·mol-1,Cu的摩尔质量为64g·mol-1,因此混合物中一定含有的金属为Al,故选项C正确;
,解得a=41.5。所以两种金属混合,要求金属折算成+2价后,一种金属的摩尔质量大于41.5g/mol,另一种小于41.5 g/mol,Zn的摩尔质量为65g·mol-1,Fe的摩尔质量为56g·mol-1,Al与盐酸反应后生成AlCl3,Al显+3价,转化成+2价,Al的摩尔质量为18g·mol-1,Cu的摩尔质量为64g·mol-1,因此混合物中一定含有的金属为Al,故选项C正确;
答案为C。


 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
【题目】将标准状况下的a L NH3完全溶于1 L水,得到体积为V L、密度为b gcm-3(b<1)、物质的量浓度为c molL-1、溶质质量分数为w的氨水(溶质按NH3算 ),下列叙述中错误的是
A.c = ![]()
B.w=![]() ×100%
×100%
C.若将该氨水蒸发出部分水(不考虑溶质NH3的逸出),使溶液质量变为原来一半,则浓度大于2c
D.上述溶液中再加入V L水 ,所得溶液的质量分数小于0.5w
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)![]() 2AB3(g) 化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)。下列判断正确的是( )
2AB3(g) 化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)。下列判断正确的是( )

A. 在T2和n(A2)不变时达到平衡,AB3的物质的量大小 为:c>b>a
B. 若T2>T1,则正反应一定是放热反应
C. 达到平衡时A2的转化率大小为:b>a>c
D. 若T2>T1,达到平衡时b、d点的反应速率为vd>vb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X元素的1个原子失去2个电子转移到Y元素的2个原子中去,形成离子化合物Z,下列说法中不正确的是( )
A. Z在熔化状态下可以导电B. Z可以表示为XY2
C. X形成+2价阳离子D. Z中存在共价键,Z可以电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 含有金属元素的化合物一定是离子化合物
B. IA族和VIIA族元素原子化合时,一定生成离子键
C. 由非金属元素形成的化合物一定不是离子化合物
D. 活泼金属与活泼非金属化合时,能形成离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀H2SO4、NaOH溶液等试剂)
(1)操作a的名称为___________,所需要的玻璃仪器为________________________。
(2)固体E的成分为_________________,加入的试剂④为________________,发生的化学方程式为__________________________________________。
(3)加入试剂①的目的是______________________________________________________。
(4)从溶液D和溶液G中得到FeSO4.7H2O晶体的操作为_____________、冷却结晶、________、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12.某溶液中含有Cl-、Br-和CrO42-浓度均为0.010mol.L-1,向该溶液中逐滴加入0.010mol.L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( )
A. Cl-、Br-、CrO42- B. CrO42-、Br-、Cl-
C. Br-、Cl-、CrO42- D. Br-、CrO42-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达平衡,平衡常数K=![]() 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
A、该反应的焓变为正值
B、恒温恒容下,增大压强,H2浓度一定减小
C、升高温度,逆反应速率减小
D、该反应化学方程式为CO+H2O=CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃下列四种溶液:①c(H+)=10-3mol·L-1的醋酸;②pH=5 的NH4Cl溶液; ③pH=10的Na2CO3溶液;④c(OH-)=10-3mol·L-1氨水溶液。由水电离出的氢离子浓度之比为 ( )
A. 1∶106∶10∶1 B. 1∶106∶107∶1
C. 108∶106∶10∶1 D. 108∶106∶107∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com