
【题目】(17分)顺丁橡胶、制备醇酸树脂的原料M以及杀菌剂N的合成路线如下:
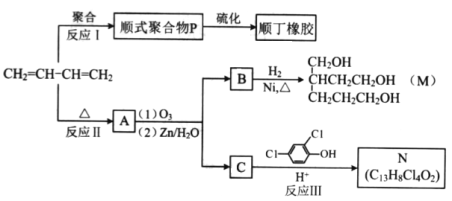
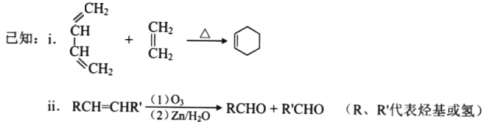
(1)CH2=CH-CH=CH2的名称是_______;
(2)反应I的反应类型是(选填字母)_______;
a.加聚反应 b.缩聚反应
(3)顺式聚合物P的结构式是(选填字母)_______;
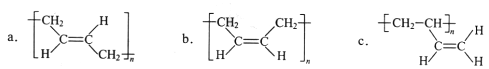
(4)A的相对分子质量为108.
①反应II的化学方程式是_____________________
②1molB完全转化为M所消耗的H2的质量是______g。
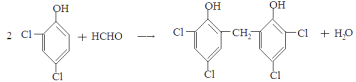
(5)反应III的化学方程式是______________________________。
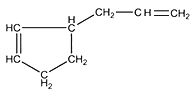
(6)A的某些同分异构体在相同反应条件下也能生成B和C,写出其中一种同分异构体的结构简式__________。
【答案】(1)1,3-丁二烯(2)a;(3)b;
①2CH2=CH-CH=CH2→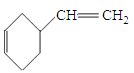 ;② 6;
;② 6;
(5) 
(6)
【解析】
试题由转化关系图可知,1,3-丁二烯发生聚合反应I得到顺式聚合物P为聚顺1,3-丁二烯;由题给信息i可知加热条件下发生反应II(双烯合成)生成A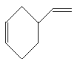 ,环己烯再发生ii的反应生成B
,环己烯再发生ii的反应生成B 和C(HCHO)。C甲醛与二氯苯酚发生反应(酚羟基邻位与甲醛结合)生成N为
和C(HCHO)。C甲醛与二氯苯酚发生反应(酚羟基邻位与甲醛结合)生成N为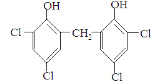 , 由此可知:
, 由此可知:
(1)根据系统命名法可知,该物质为1,3-丁二烯;
(2)反应I 的类型是加聚反应,选a;
(3)顺式P的结构简式应该是两个H原子位于双键同侧,答案为b;
(4)A为 ,反应II的化学方程式为2CH2=CH-CH=CH2→
,反应II的化学方程式为2CH2=CH-CH=CH2→ ;
;
1molB( )中含有3mol醛基,故可与3molH2发生加成生成M,消耗氢气6g;
)中含有3mol醛基,故可与3molH2发生加成生成M,消耗氢气6g;
(5)反应III 是C(甲醛)与二氯苯酚发生反应(酚羟基邻位与甲醛结合)生成N为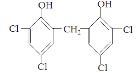 ,故化学方程式为:
,故化学方程式为:
(6)根据信息ii可知烯烃中的碳碳双键被氧化为-CHO,生成物B为 ,C为甲醛,故也可由下面的烯烃(A的一种同分异构体)
,C为甲醛,故也可由下面的烯烃(A的一种同分异构体)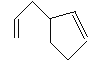 氧化得到,故答案为
氧化得到,故答案为 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】将100 mL稀硝酸和稀硫酸的混合酸溶液平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g铜粉(假设此时硝酸只被还原为NO,下同);向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化如图所示。则下列判断中错误的是
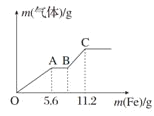
A.OA段产生的气体是NO,BC段产生的气体是H2
B.A点对应消耗NO3-物质的量为0.2 mol
C.B点对应消耗铁粉的质量为8.4 g
D.原混合酸溶液中H2SO4的浓度为4.0 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是一些元素的信息,其中有一种元素不在短周期。
元素A | 元素B | 元素C | 元素X | 元素Y |
单质是一种常见金属,与元素X形成黑色和红棕色三种常见化合物 | 基态原子M层p轨道上有5个电子 | 短周期中金属性最强,与X反应能生成两种常见化合物 | 最外层电子数是内层电子数的3倍,能形成双原子阴离子 | 单质为双原子分子,结构中σ键与π数目比为1:2 |
根据上述信息回答下列问题:
(1)写出X3的等电子体_____(写一个即可),基态Y原子核外电子所占据的最高能级的电子云形状为______。
(2)A元素在元素周期表中的___区,基态A原子的未成对电子有___个。
(3)B、C、X的简单离子半径由大到小的顺序为______(填离子符号)。
(4)HX与HY两种共价键中,键的极性较强的是____,键长较长的是____(X、Y用元素符号表示)。
(5)Y与碳元素形成的一种阴离子与Y2是等电子体,请写出该阴离子的电子式___。Y的常见氢化物易溶于水的主要原因是___。
(6)铂丝蘸取化合物CB在酒精灯上灼烧,火焰呈___色,显色原因是___(填序号)。
A.CB受热挥发 B.CB受热分解
C.C离子中电子跃迁 D.B离子中电子跃迁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于碳碳双键(![]() )中的π键不能自由旋转,因此
)中的π键不能自由旋转,因此 ![]() 和
和 是两种不同的化合物,互为顺反异构体。则分子式为C3H4Cl2的化合物的烯类异构体有
是两种不同的化合物,互为顺反异构体。则分子式为C3H4Cl2的化合物的烯类异构体有
A. 5种B. 6种C. 7种D. 8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式如下:

这种材料可采用如图所示的合成路线
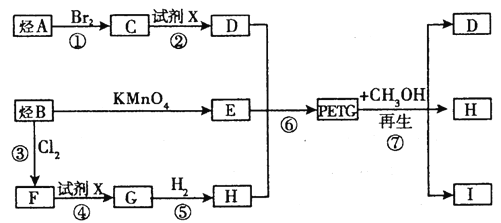
(1)![]()
(2)RCOORl+R2OH→RCOOR2+R1OH(R、R1、R2表示烃基)
试回答下列问题:
(1) ⑦的反应类型是________________。
(2) 写出I的结构简式:___________________。
(3) 合成时应控制的单体的物质的量:n(H)∶n(E)∶n (D)=____________(用m、n表示)。
(4) 写出反应②的化学方程式:______________________
(5) 写出同时符合下列两项要求的E的所有同分异构体的结构简式。
①该同分异构体的苯环上相邻的三个碳原子上都连有取代基。
②该同分异构体在一定条件下能发生银镜反应和水解反应,遇到FeCl3溶液显紫色。
______________、_________________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下图所示原电池装置的说法错误的是( )
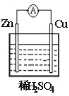
A.Zn为负极,反应为Zn-2e-=Zn2+B.铜棒上发生还原反应
C.电子从锌片经导线流向铜片D.溶液中氢离子浓度保持不变,溶液中SO42-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A.将0.1mol CO2溶于适量的水,溶液中CO32-、HCO3-、H2CO3离子总数为0.1NA
B.在7.8gNa2O2与Na2S的混合物中,离子总数为0.3NA
C.使0.5mol乙烯被溴的四氯化碳溶液完全吸收,断裂的共价键总数为0.5NA
D.标准状况下,2.24L Cl2与CH4反应完全,生成物中气体分子数目小于0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)下列关于金属及金属键的说法不正确的是______。(填字母代号)
a.金属键没有方向性与饱和性
b.金属键是金属原子与自由电子间的相互作用
c.金属熔沸点不同的原因可以用金属键强弱解释
d.电子气理论可解释金属材料的延展性,不能解释金属有良好的导电性
(2)钒广泛用于催化及钢铁工业,基态钒原子的价层电子排布图为_________________。
(3)二茂铁又叫双环戊二烯基铁[Fe(C5H5)2],熔点是172.5~173 ℃,100 ℃以上升华,二茂铁属于_____晶体。已知分子中的大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为![]() )。已知二茂铁的每个茂环带有一个单位负电荷,则每个环中的大π键应表示为________________。
)。已知二茂铁的每个茂环带有一个单位负电荷,则每个环中的大π键应表示为________________。
(4)铜可以形成一种离子化合物[Cu(NH3)4(H2O)2]SO4,若要确定[Cu(NH3)4(H2O)2]SO4是晶体还是非晶体,最科学的方法是对其进行______实验,其中阴离子的空间构型是_____,该化合物加热时首先失去的组分是H2O,原因是_______________________。
(5)最近发现,只含镁、镍和碳三种元素的晶体也具有超导性,该物质形成的晶体的立方晶胞结构如图所示。
①与Mg紧邻的Ni有________个。
②原子坐标参数可表示晶胞内部各原子的相对位置。该晶胞中原子的坐标参数为a为(0,0,0);b为(1/2,1/2,0);d为(1,1,1)。则c原子的坐标参数为_______。
③若晶胞中Ni、Mg之间的最短距离为a pm,阿伏加德罗常数的值为NA,则晶体的密度ρ=______g·cm-3(用含a、NA的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种高效、广谱、安全的杀菌、消毒剂,易溶于水。制备方法如下:
(1)步骤Ⅰ:电解食盐水制备氯酸钠。用于电解的食盐水需先除去其中的 Ca2+、Mg2+、SO42-等杂质。在除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的________和NaOH,充分反应后将沉淀一并滤去。
(2)步骤Ⅱ:将步骤Ⅰ得到的食盐水在特定条件下电解得到氯酸钠(NaClO3),再将它与盐酸反应生成ClO2与Cl2,ClO2与Cl2的物质的量比是____________。
(3)学生拟用左下图所示装置模拟工业制取并收集ClO2,用NaClO3和草酸(H2C2O4)恒温在60℃ 时反应制得。

反应过程中需要对A容器进行加热,加热的方式为____________;加热需要的玻璃仪器除酒精灯外,还有_________________;
(4)反应后在装置C中可得亚氯酸钠(NaClO2)溶液。已知NaClO2饱和溶液在温度低于38℃时,析出的晶体是NaClO2·3H2O,在温度高于38℃时析出的是NaClO2。根据右上图所示NaClO2的溶解度曲线,请完成从NaClO2溶液中制得NaClO2·3H2O的操作步骤:
①_____________;②_______________;③洗涤;④干燥。
(5)目前我国已成功研制出利用NaClO2制取二氧化氯的新方法,将Cl2通入到NaClO2溶液中。现制取270kg二氧化氯,需要亚氯酸钠的质量是________。
(6)ClO2和Cl2均能将电镀废水中的剧毒CN-氧化为无毒物质,自身被还原为Cl-。处理含CN-相同量的电镀废水,所需Cl2的物质的量是ClO2的_______倍。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com