
������������������������������Ҫ��Ӧ�ã�������ʹ�ø���IJ��Ǵ����������ǺϽ�
��1�������ӷ�Ӧ�ѵ��Ƚ������õ����ƼغϽ��䳣������ ̬��������Һ���̣������Ƶ����ʵ�������Ϊ20%��0.2mol�Ĵ˺Ͻ�ȫ�ؼ��뵽��ˮ��D2O���У���������������������������Ϊ ��
��2��þ���Ͻ��Ǿ������������ʺϽ𡣼�һ��Ͻ��ڿ�����ȼ�գ�������MgO��Al2O3�⣬���п������ɵĵ��������ʵĵ���ʽ�� ����һ��5.1g��þ���Ͻ�Ƭ����3.6 mol��L-1��200ml ��������Һ�У����������1 mol��L-1������������Һ����� mL�������������ٸı䣬��������������0.5mol �ĵ��ӷ���ת�ƣ���Ͻ���Mg�����ʵ�������Ϊ ��
��3������һ��ͭ�ĺϽ�ͭ���ɿ�����Cu��Zn�����ɷֱ������ܷ�����ܷ�����������ֽ��������аѸúϽ�Ͷ�뵽ϡ�����У����ֲ������ݵ��ٶȱ���п�����ᷴӦ���������ٶȿ죬��ԭ���� ��
��Ϊ����ijͭ�Ͻ�ijɷ֣����Ὣ����ȫ�ܽ����NaOH��Һ��pH����pH��3.4ʱ��ʼ���ֳ������ֱ���pHΪ7.0��8.0ʱ���˳����������ͼ��Ϣ�ƶϸúϽ��г�ͭ��һ������ ��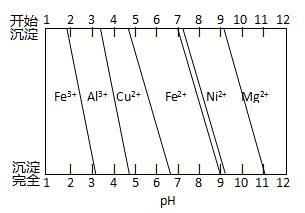
(1)Һ 0.2NA ��2��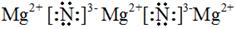 1440��50%
1440��50%
(3)��ͭп�Ͻ�����γ�ԭ��أ��ӿ컯ѧ��Ӧ���ʡ� ��Al��Ni
���������������1���ƼغϽ��䳣������Һ̬���Ƶ����ʵ�������Ϊ20%��0.2mol�Ĵ˺Ͻ����ƺͼص����ʵ����ֱ���0.04mol��0.16mol�����ݷ���ʽ2Na��2H2O��2NaOH��H2������֪����ˮ��Ӧ�������������ʵ����ֱ���0.02mol��0.08mol��������0.10mol���������������D2�������к�����������2�������Բ�������������������������Ϊ0.2NA��
��2������þ���뵪����Ӧ���ɵ���þ���������к��д����ĵ��������Ե���������Ӧ���ǵ���þ������þ�����ӻ��������ʽΪ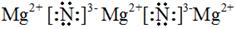 �����������ٷ����仯ʱ����ʱǡ�÷�Ӧ����������þ��������������������Һ��ֻ���������ƣ����ʵ�����3.6mol/L��0.2L��0.72mol����ؽ����������غ��֪��������Ҫ�������Ƶ����ʵ�����0.72mol��2��1.44mol������Һ���Ϊ1.44mol��1.0mol/L��1.44L��1440ml����Ͻ���Mg��Al�����ʵ����ֱ�Ϊx��y����2x+3y��0.5mol��24g/mol��x+27g/mol��y��5.1g�����x��y��0.1mol����˺Ͻ���Mg�����ʵ�������Ϊ50%��
�����������ٷ����仯ʱ����ʱǡ�÷�Ӧ����������þ��������������������Һ��ֻ���������ƣ����ʵ�����3.6mol/L��0.2L��0.72mol����ؽ����������غ��֪��������Ҫ�������Ƶ����ʵ�����0.72mol��2��1.44mol������Һ���Ϊ1.44mol��1.0mol/L��1.44L��1440ml����Ͻ���Mg��Al�����ʵ����ֱ�Ϊx��y����2x+3y��0.5mol��24g/mol��x+27g/mol��y��5.1g�����x��y��0.1mol����˺Ͻ���Mg�����ʵ�������Ϊ50%��
��3��������п�Ľ�����ǿ��ͭ��ͨ�뵽�����У�ͭп�Ͻ�����γ�ԭ��أ��ӿ컯ѧ��Ӧ���ʡ�
����ͼ��֪�����������Ϣ��֪��ʼ���ֳ���ΪAl��OH��3��pH��8.0ʱ���˳�ȥNi��OH��2����˸�ͭ�Ͻ��л���Al��Ni��
���㣺����������Ͻ����������ʡ����ݷ���ʽ���е��йؼ����Լ��ܽ�ƽ���Ӧ��


 ��ս100��Ԫ����Ծ�ϵ�д�
��ս100��Ԫ����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
������[KAl(SO4)2��12H2O]�Ʊ�Al��K2SO4��H2SO4���������£�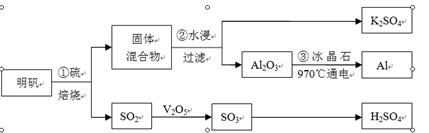
�������յĻ�ѧ����ʽΪ��4KAl(SO4)2��12H2O+3S��2K2SO4 +2Al2O3+9SO2��+48H2O
��ش��������⣺
��1���ڱ��������ķ�Ӧ�У��������� ��
��2��������У�Ϊ��߽����ʣ��ɲ�ȡ�Ĵ�ʩ�� ��
| A������������� | B�������¶� | C�����Ͻ��� | D�����̽���ʱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����������������������������������������������ȣ�Ϊԭ���Ʊ�����{�ɱ�ʾΪFe2(OH)n(SO4)3-n/2�����̷�(FeSO4.7H2O)���гɱ��͡���Ӧ�졢��Ʒ�����ߵ��ŵ㡣�Ʊ���������ͼ��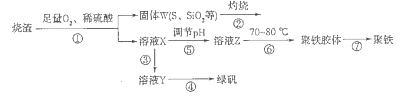
��1������ͼ����ҺXΪFe(SO4)3����Һ���ݴ�д��������������������ԭ��Ӧ�����ӷ���ʽ��____________��
��2�������ڵĴ������ڱˣ��ñ���_____________��������W��KOH��Һ���ϼ��ȣ�����һ����Ӧ�Ļ�ѧ����ʽΪ3S+6KOH 2K2S+K2SO3+3H2O���÷�Ӧ���������뻹ԭ������֮��Ϊ___________��
2K2S+K2SO3+3H2O���÷�Ӧ���������뻹ԭ������֮��Ϊ___________��
��3����������Ҫ��������ʣ��Լ�����_________��Ŀ����___________________________��
��4����������ʹ��ҺpH___________�������С������
��5�����������¶�Ϊ70 -80���Ŀ����_________________________________________ ��
��6��˫��ˮ�����Ի��������ᣩ����һ��ǿ�����������Խ������������������������Ƶ�Fe2(OH)n(SO4)3-n/2����Ӧ�Ļ�ѧ����ʽΪ__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����������(FeC6H6O7)��һ�������յĸ�Ч���Ƽ��������̷�(FeSO4��7H2O)ͨ�����з�Ӧ�Ʊ���
FeSO4��Na2CO3=FeCO3��Na2SO4
FeCO3��C6H8O7=FeC6H6O7��CO2��H2O
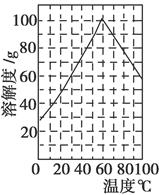
�±��г�����ؽ������������������������pH(��ʼ������pH����������Ũ��Ϊ1.0 mol��L��1����)��
| �������� | ��ʼ������pH | ������ȫ��pH |
| Fe3�� | 1.1 | 3.2 |
| Al3�� | 3.0 | 5.0 |
| Fe2�� | 5.8 | 8.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
FeԪ���ǵؿ�����ḻ��Ԫ��֮һ���ڽ����к������������������仯�����������������й㷺Ӧ�á���ش��������⡣
��1���������ǹ�ҵ��ұ������ԭ��֮һ����ԭ����Fe3O4��4CO 3Fe��4CO2������1 mol Fe3O4�μӷ�Ӧ��ת�Ƶ��ӵ����ʵ�����________ mol��
3Fe��4CO2������1 mol Fe3O4�μӷ�Ӧ��ת�Ƶ��ӵ����ʵ�����________ mol��
��2�����������ƣ�������Ҳ��������ˮ������ʹ��ʱ����������������ʹ���Է�ˮ�е������������ȥ����ԭ����___________________________________________________��
��3��ij����С�齫��ͼ��ʾװ�ð�һ��˳�����ӣ���ʵ��������ȡһ������FeCl3(��ͨ�����������ַ�Ӧ)��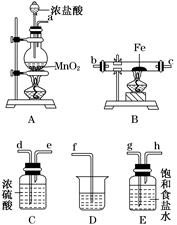
��ش��������⣺
�ٸ�װ�õ���ȷ����˳��Ϊ(��дװ�ô���)
A��________��________��________��D��
��װ��C��������_______________________________________________________��
�۷�Ӧ��ʼ��B��Ӳ�ʲ������ڵ�����Ϊ________�����Լ����������к���Fe3�����Լ���________(��д�Լ�����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�Ȼ����dz�����ˮ������,��ˮFeCl3����������ҵ���Ʊ���ˮFeCl3��һ�ֹ�����ͼ��ʾ:
��1�����������������ռ�XӦ�� ������ĸ��ţ���
a.NaOH��Һ b.����ʳ��ˮ c.FeCl2��Һ d.����KI��Һ
��2��ȡ0.5 mL����FeCl3��Һ����50 mL��ˮ��,�ú��ɫ������������,������Ӧ�����ӷ���ʽΪ ��
��3��ʵ�����д�FeCl3��Һ�Ƶ�FeCl3��6H2O����Ĺ�����,���ȼ��� �ұ��ֹ���,Ȼ����еIJ�������Ϊ ����ȴ�ᾧ�����ˡ�
��4����H2S����ͨ��FeCl3��Һ�л���ֻ���,���䷴Ӧ�����ӷ���ʽΪ ��
��5������������ԭҺ�������һ�ֵͳɱ��Ĵ��ܵ��,��ؽṹ��ͼ��ʾ���缫����Ϊʯī��,����ԭ��Ϊ:Fe3++Cr2+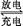 Fe2++Cr3+
Fe2++Cr3+
���طŵ�ʱ,Cl-������ ���������������;���ʱ,�����ĵ缫��ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij�о�С�齫һ����������·�徭Ũ�����ϡ���ᴦ����õ�һ�����Һ,���к���Cu2+��Fe2+��Fe3+��Al3+�Ƚ�������,��������������������Էֱ���ȡCuSO4��5H2O�����AlCl3
��Һ: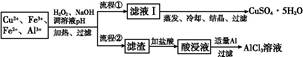
��֪:��ؽ������ӿ�ʼ��������ȫ����ʱ��pH��ΧΪ:
| ���� | Fe3+ | Fe2+ | Al3+ | Cu2+ |
| pH��Χ | 2.2��3.2 | 5.5��9.0 | 4.1��5.0 | 5.3��6.6 |
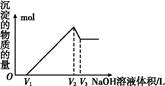
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�Ի�ͭ��(��Ҫ�ɷ���CuFeS2,����������SiO2)Ϊԭ����ͭ�ķ�����Ϊ������ͭ��ʪ����ͭ���֡�������,ʪ����ͭ�����½�չ,��ѧ�ҷ�����һ��ϸ��������ˮ��Һ������������,���Խ���ͭ��������������:4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O��ij�������ø�ԭ������ͭ���̷��Ĺ�������:
4CuSO4+2Fe2(SO4)3+2H2O��ij�������ø�ԭ������ͭ���̷��Ĺ�������: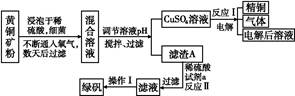
�ش���������:
(1)���������п����������������е�����ҺpH������������(�����)��
| A��Cu�� | B��Cu2(OH)2CO3�� | C��H2SO4�� | D��Fe��E.CuO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij�����ĵ�������к���ͭ�����Ƚ��������Ϊʵ����Դ�Ļ������ò���Ч��ֹ������Ⱦ��������¹������̣�
��1����������H2O2��Ŀ���� ����pH�����м�����Լ������ ���ѧʽ����ʵ���ҽ��й��˲������õ��IJ��������� ��
��2�����CuSO4��Һ��ԭ���� ����CuSO4��Һ�м���һ������NaCl��Na2SO3���������ɰ�ɫ��CuCl������д���÷�Ӧ�Ļ�ѧ����ʽ ��
��3����ȡ���Ʊ���CuCl��Ʒ0.2500g����һ������0.5mol��L-1FeCl3��Һ�У�����Ʒ��ȫ�ܽ��ˮ20mL����0.1000mol��L-1��Ce��SO4��2��Һ�ζ��������յ�ʱ����Ce��SO4��2��Һ25.00mL���йصĻ�ѧ��ӦΪ��Fe3����CuCl��Fe2����Cu2����Cl����Ce4����Fe2����Fe3����Ce3���������CuCl��Ʒ���������� ��
��4��Fe3+����ˮ�ⷴӦFe3����3H2O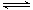 Fe(OH)3��3H�����÷�Ӧ��ƽ�ⳣ������ʽΪ ��
Fe(OH)3��3H�����÷�Ӧ��ƽ�ⳣ������ʽΪ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com