
【题目】H2S水溶液中存在电离平衡H2S![]() H++HS和HS
H++HS和HS![]() H++S2。若向H2S溶液中
H++S2。若向H2S溶液中
A. 滴加新制氯水,平衡向左移动,溶液pH减小
B. 加水,平衡向右移动,溶液中氢离子浓度增大
C. 通入过量SO2气体,平衡向左移动,溶液pH增大
D. 加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
科目:高中化学 来源: 题型:
【题目】将4mol 甲烷与氯气发生取代反应,待反应完全后测知四种取代物物质的量相同,测消耗的氯气有( )
A.2mol B.10mol C.7.5mol D.6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铷的叙述正确的是( )
A. 它位于周期表中第4周期
B. 氢氧化铷是弱碱
C. 在钠、钾、铷三种单质中,铷的熔点最高
D. 硝酸铷是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列每组的三种物质中,两边的固体均有导线连接,插入中间的液体中,其中能组成原电池的是
A. Zn | H2SO4(稀) | CB. Cu | 酒精 | Ag
C. Zn | CCl4 | CuD. Fe | H2SO4(稀) | Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,下列叙述不是可逆反应A(g)+3B(g)![]() 2C(g)达到平衡状态标志的是
2C(g)达到平衡状态标志的是
①C生成的速率与C分解的速率相等;②单位时间内生成a mol A,同时生成3a mol B;③A、B、C的浓度不再变化;④A、B、C的压强不再变化;⑤混合气体的总压强不再变化;⑥混合气体的物质的量不再变化;⑦单位时间内消耗a mol A,同时生成3a mol B;⑧A、B、C的分子数之比为1∶3∶2
A. ①⑥ B. ②④ C. ③⑧ D. ②⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种元素,它们的相关信息如表:
元素代号 | 相关信息 |
A | 最外层的电子数是次外层电子数的3倍 |
B | 质子数为11的元素 |
C | L层得1个电子后成为稳定结构 |
D | 二价阴离子核外有18个电子 |
E | 失去一个电子后就成为一个质子 |
F | 其离子与氩原子电子层结构相同,它失去一个电子后呈中性 |
(1)A原子的电子式为____。
(2)B离子的结构示意图为_____。
(3)C原子中能量最高的电子位于____(填符号)电子层。与C离子质子数与电子数均相同的微粒可能是____(用微粒符号表示)。
(4)D元素的某种同位素原子质量数为34,该原子核内的中子数为_____。
(5)E原子的质量数是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,水的电离达到平衡:H2O![]() H++OH- ΔH>0,下列叙述正确的是
H++OH- ΔH>0,下列叙述正确的是
A. 向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B. 向水中加入少量CH3COOH,平衡逆向移动,c(H+)降低
C. 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
D. 将水加热,KW增大,c(H+)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化钒(VO2)是一种新型热敏材料。+4价的钒化合物在弱酸性条件下易被氧化。实验室以V2O5为原料合成用于制备VO2的氧钒(Ⅳ)碱式碳酸铵晶体,过程如下:

回答下列问题:
(1) VOC12中V的化合价为 ________。
(2)步骤i中生成VOC12的同时生成一种无色无污染的气体,该化学方程式为___。也可只用浓盐酸与V2O5来制备VOC12溶液,该法的缺点是 _______
(3)步骤ii可在下图装置中进行。
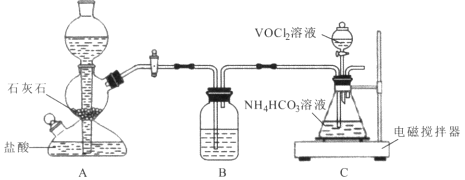
①反应前应通入CO2数分钟的目的是 ________。
②装置B中的试剂是____。
(4)测定氧钒(IV)碱式碳酸铵晶体粗产品中钒的含量。
称量ag样品于锥形瓶中,用20mL蒸馏水与30 mL混酸溶解后,加0.02 mol/LKMnO4溶液至稍过量,充分反应后继续加1 %NaNO2溶液至稍过量,再用尿素除去过量的NaNO2,最后用c mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗体积为b mL。滴定反应为:VO2++Fe2++2H+= VO2++Fe3++H2O.
①KMnO4溶液的作用是_______ 。NaNO2溶液的作用是______ 。
②粗产品中钒的质量分数的表达式为_________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫是一种很活泼的元素,在适宜的条件下能形成2、+6、+4、+2、+1价的化合物。
Ⅰ.焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一,带有强烈的SO2气味,久置于空气中易被氧化,其溶于水生成的NaHSO3溶液呈酸性。某研究小组采用如图所示装置(实验前已除尽装置内的空气)制取Na2S2O5。
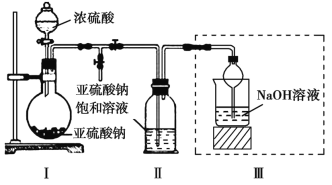
(1)装置Ⅰ中的浓硫酸____(能或不能)用稀硫酸代替,原因是______________________________________________。
(2)装置Ⅱ中有Na2S2O5晶体析出,要获得已析出的晶体,可采取的操作是__________。
(3)设计检验Na2S2O5晶体在空气中变质的实验方案:_______________。
Ⅱ.Na2S2O3溶液可以用于测定溶液中ClO2的含量,实验方案如下。
步骤1:准确量取ClO2溶液10.00 mL,稀释至100 mL。
步骤2:量取V1 mL稀释后的ClO2溶液于锥形瓶中,调节溶液的pH≤2,加入足量的KI晶体,摇匀,在暗处静置30分钟。(已知:ClO2+I+H+![]() I2+Cl+H2O 未配平)
I2+Cl+H2O 未配平)
步骤3:以淀粉溶液作指示剂,用c mol·L1 Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知:I2+2S2O32—=2I+ S4O62—)
(1)准确量取10.00 mL ClO2溶液的玻璃仪器是____________。
(2)确定滴定终点的现象为________________________________。
(3)根据上述步骤计算出原ClO2溶液的物质的量浓度为____mol·L1(用含字母的代数式表示)。
(4)下列操作会导致测定结果偏高的是_______________ (填字母)。
A.未用标准浓度的Na2S2O3溶液润洗滴定管
B.滴定前锥形瓶中有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.读数时,滴定前仰视,滴定后俯视
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com