
下列说法错误的是 ( )
A.钠是电和热的良导体
B.饱和溶液的碱性:NaHCO3大于Na2CO3
C.明矾净水是由于明矾在水中形成Al(OH)3胶体具有吸附作用
D.某溶液焰色反应时,如果火焰呈黄色就说明该溶液一定有钠元素,可能有钾元素
科目:高中化学 来源: 题型:
将二氧化硫通入溴水中发生如下的反应:SO2+Br2+2H2O═2HBr+H2SO4,反应中转移的电子数和还原剂是( )
|
| A. | 2e﹣,H2SO4 | B. | 4e﹣,SO2 | C. | 2e﹣,Br2 | D. | 2e﹣,SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
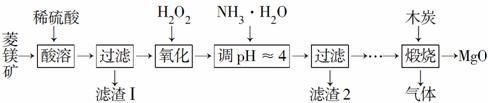
(1)MgCO3与稀硫酸反应的离子方程式为___________________ _____________________________________________________________________________________________________________________________。
(2)加入H2O2氧化时,发生反应的化学方程式为________________________________________________________________________________________________________________________________________________。
(3)滤渣2的成分是____________________________________________ _________________________(填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C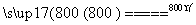 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C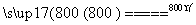 MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C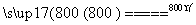 MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用如图装置对煅烧产生的气体进行分步吸收或收集。
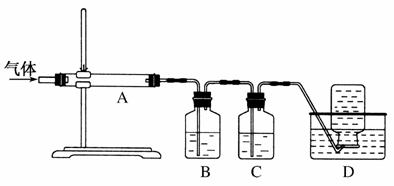
①D中收集的气体是________(填化学式)。
②B中盛放的溶液可以是________(填字母)。
a.NaOH溶液 b.Na2CO3溶液
c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体能与热的NaOH溶液反应,产物中元素的最高价态为+4,写出该反应的离子方程式:
___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
明矾石的主要成分是K2SO4·Al2(SO4)3·2Al 2O3·6H2O,此外还含有少量Fe2O3杂质。利用明矾石来制备Al2O3、K2FeO4和H2SO4的工艺流程如下: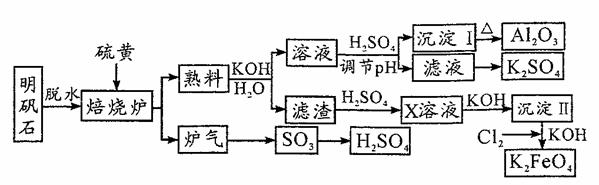
请回答下列问题:
(1)“焙烧”过程中反应的化学方程式为2Al2(SO4)3+3S =2Al2O3 +9SO2,该反应中氧化剂与还原剂的物质的量之比是 _ 。若生成102g Al2O3,转移的电子数目为 。
(2)写出化学式:沉淀Ⅰ是 ,沉淀Ⅱ是 ___________ 。
(3)熟料溶解时反应的离子方程式为______________________________________________。
(4)溶液经加硫酸调节pH后,过滤、洗涤,可得沉淀Ⅰ,证明沉淀Ⅰ已洗涤干净的实验操作和现象是 。
(5)写出Cl2将沉淀Ⅱ氧化为K2FeO4的化学方程式:
______________________________________ 。
(6)“焙烧”过程中生成的SO2可用于制H2SO4。已知25℃,101kPa时:
2SO2(g) + O2(g)  2SO3 (g) △H1=-197.0kJ•mol-1
2SO3 (g) △H1=-197.0kJ•mol-1
H2O(g)=H2O(l) △H 2=-44.0 kJ·mol-1
2SO2(g) + O2(g) + 2H2O(g) =2H2SO4 (l) △H3=-545kJ•mol-1
则SO3 (g)和H2O(l)反应的热化学方程式为 _________ 。
(7)本工艺流程中可循环物质为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体
 积的关系如右图所示,由此确定,原溶液中含有的阳离子是( )
积的关系如右图所示,由此确定,原溶液中含有的阳离子是( )
A.Mg2+、Al3+、Fe2+
B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+
D.只有Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
(1) 鉴别NaCl和Na2CO3溶液的试剂是 ,离子方程式为 。
(2) 除去混入Na2CO3溶液中少量NaHCO3杂质的试剂是 ,离子方程式为
。
(3) 除去Fe粉中少量Al粉杂质的试剂是 ,离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
A-D是中学化学实验中常见的几种温度计装置示意图,正确的是:
A.酒精和浓硫酸混合加热制乙烯 B.石油分馏实验
C.苯跟溴的取代反应 D.电石跟水反应制乙炔
| A | B | C | D |
|
|
|
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
A.脱氧过程是吸热反应 ,可降低温度,延长糕点保质期
,可降低温度,延长糕点保质期
B.脱氧过程中铁作原电池正极,电极反应为: Fe-3e→Fe3+
Fe-3e→Fe3+
C.脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e→4OH-
D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com