
【题目】下列叙述中,正确的是
A.干燥木棍不导电,但潮湿木棍导电,说明水的导电能力非常强
B.熔融的KNO3能导电,所以KNO3是电解质
C.铜丝、石墨均能导电,所以它们都是电解质
D.NaOH溶于水,在通电条件下才能发生电离
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】下列关于对各有机物的说法正确的是
A.苯分子中的所有原子均在同一平面上
B.甲烷能使酸性KMnO4溶液褪色
C.乙醇能使紫色石蕊试液变红
D.蛋白质只含有C、H、O三种元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 向氨水中不断通入CO2,随着CO2的增加,![]() 不断减小
不断减小
B. 在铜的精炼过程中,若转移1mol电子,则阳极一定溶解32gCu
C. 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)的△H>0,△S<0
D. 将下图中的活塞快速推至A处固定,气体颜色先变深、再变浅,但比起始时深

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝基苯是重要的精细化工原料,是医药和染料的中间体,还可作有机溶剂。制备硝基苯的过程如下:
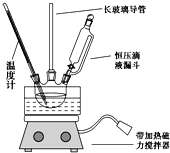
①组装如图反应装置。配制混酸,取100mL烧杯,用20mL浓硫酸与18 mL浓硝酸配制混酸,加入漏斗中,把18 mL 苯加入三颈烧瓶中。
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀。
③在50~60℃下发生反应,直至反应结束。
④除去混酸后,粗产品依次用蒸馏水和10%Na2CO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品。
已知:i.![]() +HNO3(浓)
+HNO3(浓)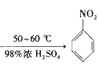 +H2O
+H2O
![]() +HNO3(浓)
+HNO3(浓)
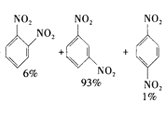 +H2O
+H2O
ii可能用到的有关数据列表如下:
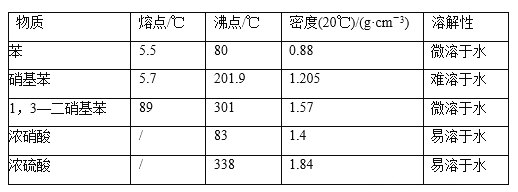
(1)配制混酸应在烧杯中先加入___________。
(2)恒压滴液漏斗的优点是_____________。
(3)实验装置中长玻璃管可用_______代替(填仪器名称).
(4)反应结束后,分离混酸和产品的操作方法为_________。
(5)为了得到更纯净的硝基苯,还需先向液体中加入___(填化学式)除去水,然后采取的最佳实验操作是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学科学的形成、发展与应用过程中,下列科学家与其成就不相对应的是
A.1961年英国科学家波义尔提出化学元素的概念
B.1774年法国科学家拉瓦锡提出燃烧的氧化学说
C.1811年意大利科学家阿伏加德罗提出原子学说
D.1943年,科学家侯德榜发明联合制碱法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示下列描述正确的是
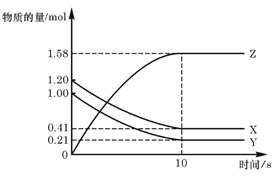
A. 反应开始到10s,用Z表示的反应速率为0.158 mol/(Ls)
B. 反应开始到10s,X的物质的量浓度减少了0.79 mol/L
C. 反应开始到10s,Y的转化率为79.0 %
D. 反应的化学方程式为:X+Y![]() Z
Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把3.0molM和2.5molN混合于2.0L的恒容密闭容器中,发生反应3M(g)+N(g)![]() xP(g)+2Q(g),5min反应达到平衡,已知M的转化率为50%,P的反应速率为0.15mol·L-1·min-1,则下列说法正确的是
xP(g)+2Q(g),5min反应达到平衡,已知M的转化率为50%,P的反应速率为0.15mol·L-1·min-1,则下列说法正确的是
A. 方程式中x=2
B. 达平衡后,容器内压强是反应起始时的2倍
C. 容器内混合气体的密度不再变化和平均相对分子质量不再变化均可作为达到化学平衡状态
D. 达新平衡时P的体积分数为25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物.下列化学反应符合“绿色化学”理念的是
A. 制CuSO4:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
B. 制Cu(NO3)2:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
C. 制CuSO4:2Cu+O2![]() 2CuO; Cu+H2SO4(稀)═CuSO4+H2O
2CuO; Cu+H2SO4(稀)═CuSO4+H2O
D. 制Cu(NO3)2:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A.O2-、F-、Na+、Mg2+半径依次减小
B.O2和O3是氧元素的同素异形体
C.同一元素的不同核素化学性质几乎完全相同
D.同主族元素含氧酸的酸性随核电荷数的增加而减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com