
【题目】下列分散系最不稳定的是
A. 向NaOH溶液中通入CO2得到的无色溶液
B. 向碘水溶液中滴加四氯化碳充分振荡后,静置后的下层液体
C. 向沸水中滴入饱和的FeCl3溶液得到的红褐色液体
D. 向CuSO4溶液中加入NaOH溶液得到的分散系
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列说法正确的是( )
A. 1 mol NaHCO3与足量盐酸反应放出CO2气体的体积为22.4L
B. 1 mol Al3+离子含有的核外电子数为3NA
C. O2和O3的混合气体,质量为48g,所含氧原子数为3NA
D. 高温下,0.2mol Fe与足量水蒸气反应,生成的H2的分子数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下列方法测定某水样中O2的含量。

(1)实验原理
用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,再用I-将生成的MnO(OH)2再还原为Mn2+,第二步反应的离子方程式为___________________。然后用Na2S2O3标准溶液滴定生成的I2。
已知:①2Mn2++O2+4OH-=2 MnO(OH)2 ②I2+2Na2S2O3=2NaI+Na2S4O6。
③S2O32-+2H+=SO2↑+S+H2O
(2)实验步骤
①打开止水夹a 和b,从A 处向装置内鼓入过量N2,此操作的目的是______________;
②用注射器抽取某水样20.00 mL从A 处注入锥形瓶;
③再分别从A 处注入含m mol NaOH溶液及过量的MnSO4溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A 处注人足量NaI溶液及含n mol H2SO4的硫酸溶液使溶液接近中性;
⑥重复④的操作。
⑦取下锥形瓶,向其中加入2~3滴________________作指示剂;
⑧用0.005 mol`L-1Na2S2O3滴定至终点。
(3)数据分析
①若在滴定过程中消耗的Na2S2O3标准溶液体积为3.60 mL,则此水样中氧气(O2)的含量为___(单位:mg·L-1)。
②若未用Na2S2O3标准溶液润洗滴定管,则测得水样中O2的含量将____________(填“偏大”、“偏小”或“不变”)。
③实验要求加入适量的H2SO4使溶液接近中性,其原因是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见物质A~K之间存在如下图所示的转化关系,其中D、E为单质,请回答下列问题(图中有些反应的产物和反应的条件没有全部标出)。

(1)写出下列物质中溶质的名称:B是 __________,G是____________
(2)反应“F→G”的化学方程式是_____________________________________________
(3)反应“J→I”的离子方程式是_____________________________________________
(4)溶液I中混有溶液J,除去J的方法是:________________________________________________________________
(5)检验溶液I中阳离子的方法是:__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M2O7x-与S2-在酸性溶液中发生如下反应:M2O7x-+3S2-+14H+2M3++3S↓+7H2O,则M2O7x-中M的化合价是( )
A. +2 B. +4 C. +6 D. +3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用98%的浓硫酸(ρ=1.84g·cm-3)配制成浓度为0.5mol·L-1的稀硫酸480ml。
若实验仪器有: A.10 mL量筒 B.20 mL量筒 C.托盘天平 D.玻璃棒
E.100 mL容量瓶 F.250 mL容量瓶 G.500 mL容量瓶 H.胶头滴管 I.200 mL烧杯
(1)所需浓硫酸的体积为______mL(保留到小数点后一位)。
(2)实验时需选用的仪器有D、I、 ______________________(填序号)。
(3)请将下列各操作,按正确的序号填在横线上(可重复使用)。
A.用量筒量取浓H2SO4;B.反复颠倒摇匀;C.用胶头滴管加蒸馏水至刻度线
D.洗净所用仪器;E.稀释浓H2SO4;F.将溶液转入容量瓶
其操作正确的顺序依次为____________________________。
(4) 配制过程中,下列操作会使配制的稀硫酸溶液浓度偏高的是(填序号)________。
①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③定容时俯视读数
④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组采用分类思想、利用抽象方程式:A+H2O→B+C总结相关物质的知识。
(1)若A为单质:
①金属氧化物B常作为磁性材料,则元素A在周期表中的位置为_________。
②A是一种黄绿色气体单质,则生成物中弱电解质的结构式为_________。
③B能腐蚀玻璃,单质C为空气的主要成分之一,写出该反应的化学方程式: _________。
(2)若A为氧化物:
①A为淡黄色固体,则A的电子式为_________。
②A、C均能造成光化学烟雾,则生成1molB转移的电子数目为_________。
(3)若B俗称酒精,C是生活中食用醋的主要成分,则有机物A的名称是_________。另外,A为盐时还可能发生盐类的水解,用以总结水解的规律及微粒浓度的关系等知识。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃A,标准状况下的密度为1.25g/L.B和D都是生活中常见的有机物,D能跟碳酸氢钠反应,E有香味.它们之间的转化关系如图1所示: 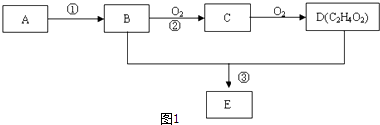
(1)A的电子式为 , D中官能团的名称为 .
(2)以A为原料自身合成高分子化合物的化学方程式为 , 反应类型是 .
(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图2所示).观察到的现象是 , 重复操作2﹣3次.写出过程②反应方程式 . 
(4)B、D在浓硫酸的作用下实现反应③,实验装置如图3所示: 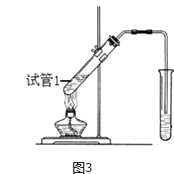
①试管1中实现反应③的化学方程式为 ,
②反应开始时用酒精灯对试管小火加热的原因是: . (已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.NO2、SO2、BF2、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构
B.P4和CH4都是正四面体分子且键角都为109°28ˊ
C.NaCl晶体中与每个Na+距离相等且最近的Na+共有8个
D.单质的晶体中一定不存在的微粒是阴离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com