
【题目】常温下,有pH=1的某溶液中可能含有Na+、Fe2+、Fe3+、I﹣、Cl﹣、CO32﹣中的某几种,现取100mL该溶液进行如下实验: 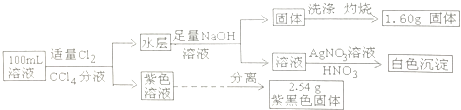
根据实验结果,下列判断正确的是( )
A.Fe2+、I﹣、Cl﹣三种离子一定存在
B.不能确定Na+和Cl﹣是否存在,CO ![]() 一定不存在
一定不存在
C.Fe3+与Fe2+至少有一种
D.该溶液中c(Cl﹣)≥0.1mol?L﹣1
【答案】AD
【解析】解:pH=1的溶液中氢离子浓度为0.1mol/L,100mL该溶液中含有氢离子的物质的量为0.01mol,则一定不存在CO ![]() ; 向溶液中通入氯气分液后得到紫色溶液,则原溶液中含有I﹣ , 铁离子能够氧化碘离子,则一定不存在Fe3+;2.54g为碘单质,物质的量为
; 向溶液中通入氯气分液后得到紫色溶液,则原溶液中含有I﹣ , 铁离子能够氧化碘离子,则一定不存在Fe3+;2.54g为碘单质,物质的量为 ![]() =0.01mol,原溶液中含有碘离子的物质的量为0.02mol;
=0.01mol,原溶液中含有碘离子的物质的量为0.02mol;
水层中加入氢氧化钠溶液得到固体,该固体为氢氧化亚铁,灼烧固体得到的1.60g为氧化铁,则溶液中一定存在Fe2+ , 根据铁元素守恒可知亚铁离子的物质的量为: ![]() ×2=0.02mol,0.02mol亚铁离子带有正电荷为0.04mol,0.02mol碘离子带有0.02mol电子,所以原溶液中一定含有Cl﹣ , 其物质的量至少为0.04mol﹣0.02mol﹣0.01mol=0.01mol,氯离子的浓度最小为
×2=0.02mol,0.02mol亚铁离子带有正电荷为0.04mol,0.02mol碘离子带有0.02mol电子,所以原溶液中一定含有Cl﹣ , 其物质的量至少为0.04mol﹣0.02mol﹣0.01mol=0.01mol,氯离子的浓度最小为 ![]() =0.1mol/L,
=0.1mol/L,
A.根据分析可知,原溶液中一定含有Fe2+、I﹣、Cl﹣ , 故A正确;
B.原溶液中一定不存在CO ![]() ,一定含有Cl﹣ , 故B错误;
,一定含有Cl﹣ , 故B错误;
C.原溶液中一定存在Fe2+ , 一定不存在Fe3+ , 故C错误;
D.根据分析可知该溶液中c(Cl﹣)≥0.1nolL﹣1 , 故D正确;
故选AD.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】已知c(NH4Cl)≤0.1mol/L时,溶液pH>5.1.现用0.1mol/L盐酸滴定10mL 0.05mol/L氨水,用甲基橙作指示剂,达到滴定终点,所用盐酸的体积为( )
A.10 mL
B.5 mL
C.大于5 mL
D.小于5 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对物质分类的归纳中,错误的是( )
A. 蔗糖、酒精、甲烷等这类含碳化合物属于有机物
B. 由金属离子和酸根离子组成的化合物称为盐
C. 与酸反应,只生成盐和水的氧化物,通常称为碱性氧化物
D. 能电离出氢离子的化合物一定为酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖的结构简式为CH2OH—CHOH—CHOH—CHOH—CHOH—CHO,其对应的性质中不正确的是( )
A.葡萄糖在一定条件下能水解
B.可与乙酸发生取代反应
C.能发生银镜反应
D.葡萄糖的分子式是C6H12O6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾严重影响人们的生活,汽车尾气排放是造成雾霾天气的重要原因之一.已知汽车尾气排放时容易发生以下反应:①N2(g)+O2(g)2NO(g)△H1=a kJmol﹣1
②2NO(g)+O2(g)=2NO2(g)△H2=b kJmol﹣1
③CO(g)+ ![]() O2(g)CO2(g)△H3=c kJmol﹣1
O2(g)CO2(g)△H3=c kJmol﹣1
④2CO(g)+2NO(g)N2(g)+2CO2(g)△H4
请回答下列问题:
(1)根据反应①②③,确定反应④中△H4=kJmol﹣1 .
(2)对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应①的Kp=(用表达式表示).
(3)下列情况能说明反应②已达平衡状态的是(填编号).
A.单位时间内生成1mol NO2的同时消耗了1mol NO
B.在恒温恒容的容器中,混合气体的密度保持不变
C.在恒温恒压的容器中,容器的体积保持不变
D.混合气体的平均相对分子质量保持不变
(4)反应③在(填“高温”或“低温”)下不利于自发进行.
(5)探究反应④中NO的平衡转化率与压强、温度的关系,得到如图所示的曲线.试分析实际化工生产中不采用高压的原因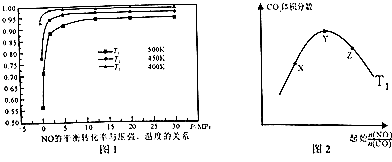
(6)探究反应④中平衡时CO2的体积分数与反应物中 ![]() 的比值、温度的关系,得到如图2所示的曲线. ①在X、Y、Z三点中,CO的转化率从大到小的顺序是 .
的比值、温度的关系,得到如图2所示的曲线. ①在X、Y、Z三点中,CO的转化率从大到小的顺序是 .
②若保持其他条件不变,请在图2中,画出温度为T2(T2<T1)时的变化趋势曲线 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
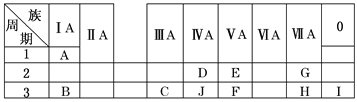
(1)表中元素,化学性质最不活泼的是________,只有负价而无正价的元素是________。
(2)C元素在元素周期表中的位置是第三周期第________族。
(3)最高价氧化物的水化物酸性最强的是________,呈两性的是________。
(4)A分别与E、G、H形成的化合物中,最稳定的是________。
(5)在B、C、E、F中,原子半径最大的是________。
(6)B、H两种元素所形成的化合物所含的化学键类型为________________。
(7)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:__________________________。
(8)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.BF3和NCl3中,每个原子的最外层都具有8电子稳定结构
B.金刚石比碘单质熔沸点高
C.NaOH熔化的过程中,既破坏了离子键又破坏了共价键
D.常温常压下,H2O是液态,H2S是气态,说明H2O的热稳定性更好
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com