
”¾ĢāÄæ”æ»ÆŗĻĪļDMPGŹĒŅ»ÖÖČĖ¹¤ŗĻ³ÉĮ×Ö¬£¬ŹĒĄķĻėµÄŅ©ÓĆÖ¬ÖŹĢåøØĮĻÖ®Ņ»”£ĘäŗĻ³ÉĀ·ĻßæÉÉč¼ĘČēĶ¼ĖłŹ¾:
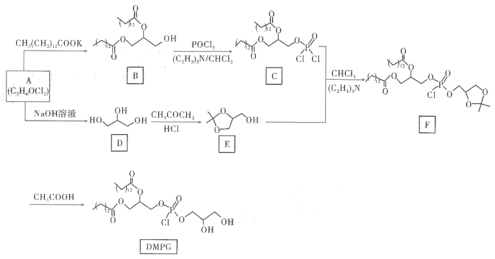
»Ų“šĻĀĮŠĪŹĢā:
£Ø1£© DĖ׳ĘøŹÓĶ£¬Ęä»ÆѧĆū³ĘĪŖ_______£»EµÄ·Ö×ÓŹ½ĪŖ______£¬Ęä¹ŁÄÜĶÅĆū³ĘĪŖ______”£
£Ø2£©AÉś³ÉDµÄ»Æѧ·½³ĢŹ½ĪŖ_______£¬·“Ó¦ĄąŠĶĪŖ_____________”£
£Ø3£©(C2H5)3NŹĒŅ»ÖÖÓŠ»ś¼ī£¬æÉĶĘ²āĘäŌŚBÉś³ÉC”¢CÓėEÉś³ÉFµÄ·“Ó¦ÖŠĘšµ½µÄ×÷ÓĆŹĒ_____”£
£Ø4£©XŹĒEµÄĶ¬·ÖŅģ¹¹Ģ壬Š“³ö·ūŗĻĻĀĮŠĢõ¼žµÄXµÄ½į¹¹¼ņŹ½__________”¢_________”£
¢ŁÄÜ·¢ÉśŅų¾µ·“Ó¦;¢ŚÄÜÓė½šŹōÄĘ·“Ӧɜ³ÉĒāĘų£¬ĒŅn(X):n( H2) =1:1;¢ŪÓŠĪåÖÖ²»Ķ¬»Æѧ»·¾³µÄĒā£¬øöŹż±ČĪŖ4:3:2:2:1”£
£Ø5£©ŅŃÖŖCH3COCH3 (±ūĶŖ)ÓėDÉś³ÉEµÄ·“Ó¦Ąś³ĢĪŖ:
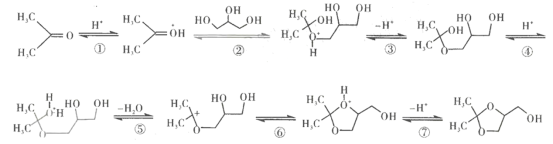
Š“³öCH3COCH3ÓėHOCH2CH2OH·“Ó¦Ąś³ĢµÄµŚ¢Ü~µŚ¢ß²½:![]() ____________
____________
”¾“š°ø”æ1,2,3-±ūČż“¼»ņ±ūČż“¼ C6H12O3 ĆŃ¼ü”¢ōĒ»ł CH2ClCHClCH2OH+2NaOH![]() HOCH2CH(OH)CH2OH+2NaCl Č”“ś·“Ó¦£ØĖ®½ā·“Ó¦£© ĪüŹÕ·“Ӧɜ³ÉµÄHCl£¬Ģįøß·“Ó¦×Ŗ»ÆĀŹ CH3C(CH2OH)2CH2CHO CH3CH3C(CH2OH)2CHO
HOCH2CH(OH)CH2OH+2NaCl Č”“ś·“Ó¦£ØĖ®½ā·“Ó¦£© ĪüŹÕ·“Ӧɜ³ÉµÄHCl£¬Ģįøß·“Ó¦×Ŗ»ÆĀŹ CH3C(CH2OH)2CH2CHO CH3CH3C(CH2OH)2CHO 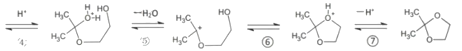
”¾½āĪö”æ
AµÄ·Ö×ÓŹ½ĪŖC3H6OCl2£¬ÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦æÉÉś³ÉøŹÓĶ£¬øĆ¹ż³ĢÓ¦ĪŖĀ±“śĢžµÄČ”“ś·“Ó¦£¬ŌņAĪŖCH2ClCHClCH2OH”£
(1)DµÄ½į¹¹¼ņŹ½ĪŖHOCH2CH(OH)CH2OH£¬øł¾ŻĻµĶ³ĆüĆū·ØæÉÖŖĘäĆū³ĘĪŖ1,2,3-±ūČż“¼»ņÕß±ūČż“¼£»øł¾ŻEµÄ¼üĻߏ½æÉÖŖEµÄ·Ö×ÓŹ½ĪŖC6H12O3£¬Ęä¹ŁÄÜĶÅĪŖĆŃ¼ü”¢ōĒ»ł£»
(2)AÉś³ÉDµÄ·“Ó¦ĪŖĀ±“śĢžµÄČ”“ś·“Ó¦£¬·½³ĢŹ½ĪŖCH2ClCHClCH2OH+2NaOH![]() HOCH2CH(OH)CH2OH+2NaCl£¬·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦(Ė®½ā·“Ó¦)£»
HOCH2CH(OH)CH2OH+2NaCl£¬·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦(Ė®½ā·“Ó¦)£»
(3)øł¾ŻBŗĶC£¬C”¢FÓėEµÄ½į¹¹¶Ō±ČæÉÖŖ£¬Į½øö·“Ó¦¾łĪŖČ”“ś·“Ó¦£¬øł¾ŻČ”“ś·“Ó¦µÄ¹ęĀÉæÉÖŖøĆ¹ż³ĢÖŠÓŠHClÉś³É£¬¶ų(C2H5)3NŹĒŅ»ÖÖÓŠ»ś¼ī£¬æÉŅŌŗĶHCl·“Ó¦£¬Ź¹Ę½ŗāÓŅŅĘŌö“ó·“Ó¦×Ŗ»ÆĀŹ£»
(4)EµÄ·Ö×ÓŹ½ĪŖC6H12O3£¬²»±„ŗĶ¶ČĪŖ1£¬ĘäĶ¬·ÖŅģ¹¹ĢåXĀś×ć£ŗ
¢ŁÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ĖµĆ÷ŗ¬ÓŠ”ŖCHO½į¹¹£»
¢ŚÄÜÓė½šŹōÄĘ·“Ӧɜ³ÉĒāĘų£¬ĒŅn(X):n( H2) =1:1ĖµĆ÷ŗ¬ÓŠōĒ»ł»ņōČ»ł£¬¶ųøĆ·Ö×ӵIJ»±„ŗĶ¶ČĪŖ1£¬ĒŅ±Ųŗ¬”ŖCHO£¬ĖłŅŌÖ»ÄÜŹĒōĒ»ł£¬ĒŅŗ¬ÓŠĮ½øöōĒ»ł£»
¢ŪÓŠĪåÖÖ²»Ķ¬»Æѧ»·¾³µÄĒā£¬øöŹż±ČĪŖ4:3:2:2:1£¬ĖµĆ÷øĆ·Ö×Ó½į¹¹¶Ō³Ę£»
ŌņĀś×ćĢõ¼žµÄĶ¬·ÖŅģ¹¹ĢåÓŠ£ŗCH3C(CH2OH)2CH2CHOŗĶCH3CH3C(CH2OH)2CHO£»
(5)øł¾ŻĢį¹©µÄŠÅĻ¢æÉÖŖ£¬CH3COCH3ÓėHOCH2CH2OHµÄ·“Ó¦Ļąµ±ÓŚCH3COCH3ÓėD[HOCH2CH(OH)CH2OH]Č„µō×īÖÕ²śĪļÖŠ»·ÉĻµÄČ”“ś»ł£¬ĖłŅŌµŚ¢Ü~µŚ¢ß²½ĪŖ£ŗ ”£
ӣ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æAÓėBŹĒ¶ĢÖÜĘŚµÄĮ½ÖÖŌŖĖŲ£¬ĖüĆĒµÄĄė×Ó![]() Óė
Óė![]() ¾ßÓŠĻąĶ¬µÄŗĖĶāµē×Ó²ć½į¹¹£¬ŌņĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ( )
¾ßÓŠĻąĶ¬µÄŗĖĶāµē×Ó²ć½į¹¹£¬ŌņĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ( )
A.Ō×ÓŠņŹżA>BB.µē×ÓŹżA>BC.Ō×Ó°ė¾¶A>BD.Ąė×Ó°ė¾¶![]() >
>![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ»śĪļ K ŹĒijŅ©ĪļµÄÖŠ¼äĢ壬ŗĻ³ÉĀ·ĻßČēĶ¼ĖłŹ¾£ŗ
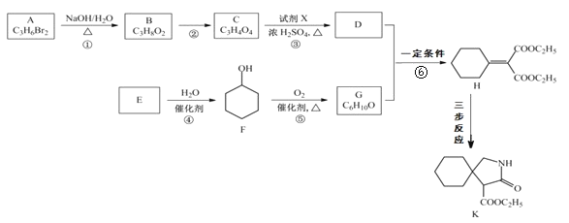
ŅŃÖŖ£ŗi.R-CN![]() R-CH2-NH2
R-CH2-NH2
ii.R1-NH2+R2COOC2H5![]()
![]() +C2H5OH
+C2H5OH
»Ų“šĻĀĮŠĪŹĢā
(1)A µÄĆū³ĘŹĒ_______”£
(2)·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½ŹĒ_____”£
(3)·“Ó¦¢ŚµÄĄąŠĶŹĒ_____”£
(4)·“Ó¦¢ŪÖŠµÄŹŌ¼Į XŹĒ_____”£
(5)E ŹōÓŚĢž£¬Ęä½į¹¹¼ņŹ½ŹĒ_____”£
(6)H ÖŠĖłŗ¬µÄ¹ŁÄÜĶÅŹĒ_____”£
(7)·“Ó¦¢ŽµÄ»Æѧ·½³ĢŹ½ŹĒ_____”£
(8)H ¾Čż²½·“Ó¦ŗĻ³É K£ŗH![]() I”śJ”śK£¬Š“³öÖŠ¼ä²śĪļ IŗĶJµÄ½į¹¹¼ņŹ½_____”£
I”śJ”śK£¬Š“³öÖŠ¼ä²śĪļ IŗĶJµÄ½į¹¹¼ņŹ½_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹ĢĢåAµÄ»ÆѧŹ½ĪŖNH5(Ņ²æÉŠ“ĪŖ£ŗNH4H)£¬ĖüµÄĖłÓŠŌ×ÓµÄ×īĶā²ć¾łĀś×ć2øö»ņ8øöµē×ÓµÄĪČ¶Ø½į¹¹”£ŌņĻĀĮŠÓŠ¹ŲĖµ·ØÖŠ“ķĪóµÄŹĒ£Ø £©
A.ĖüÓėĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖNH5 + H2O ØT NH3H2O + H2”ü
B.NH5ÖŠ¼ČÓŠ¹²¼Ū¼üÓÖÓŠĄė×Ó¼ü
C.NH5µÄµē×ÓŹ½ĪŖ 
D.1 mol NH5ÖŠŗ¬ÓŠ5NAøöN©H¼ü£ØNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ25 CŹ±£¬H2SO3µÄpKa1”¢pKa2(pK= -lgK)·Ö±šĪŖ1.89”¢7.20, NH3”¤H2OµÄpKbĪŖ4.72”£³£ĪĀŹ±,ĻĀĮŠÖø¶ØČÜŅŗÖŠĮ£×ÓĪļÖŹµÄĮæÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ
A.pH=3µÄH2SO3ČÜŅŗÖŠ£¬c(HSO3 -) +2c(SO3-)=1 ”Į10-3 mol”¤L-1
B.0.1 mol”¤L-1H2SO3ČÜŅŗÓĆNaOHČÜŅŗµĪ¶ØÖĮpH =7.20, c( HSO3 ) =2c(SO3- )
C.0.1 mol.L-1H2SO3ČÜŅŗÓĆ°±Ė®µĪ¶ØÖĮpH=7.0, c(NH4£«) =c(HSO3-) +c(SO32- )
D.0.1 mol”¤L-1NH4HSO3ČÜŅŗÖŠ: c(NH4+ ) >c(H+) >c( NH3”¤H2O)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©ĻĀĮŠŹĒ֊ѧ»Æѧ֊ŹģĻ¤µÄĪļÖŹ:
O2””½šøÕŹÆ””NaBr””H2SO4””Na2CO3””Na2S””NaHSO4
»Ų“šĻĀĮŠĪŹĢā:
ÕāŠ©ĪļÖŹÖŠ,Ö»ŗ¬¹²¼Ū¼üµÄŹĒ________;Ö»ŗ¬Ąė×Ó¼üµÄŹĒ________;¼Čŗ¬Ąė×Ó¼üÓÖŗ¬¹²¼Ū¼üµÄŹĒ________”£
£Ø2£©Š“³öĻĀĮŠĪļÖŹµÄµē×ÓŹ½”£
Na2O2£ŗ_________________£»
NH4H£ŗ_______________________£»
£Ø3£©Š“³öĻĀĮŠĪļÖŹµÄ½į¹¹Ź½”£
CO2£ŗ____________________
H2O2£ŗ_______________________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÅäÖĘĪļÖŹµÄĮæÅضČĪŖ0.1 mol”¤L£1µÄNa2CO3ČÜŅŗ100 mLŹ±£¬ĻĀĮŠ²Ł×÷ÕżČ·µÄŹĒ(””””)
A. ÓĆĶŠÅĢĢģĘ½³ĘČ”1.06 gĪŽĖ®Ģ¼ĖįÄĘ£¬ŌŚÉÕ±ÖŠ¼ÓŹŹĮæĖ®Čܽā£¬“żĄäČ“µ½ŹŅĪĀŗ󣬽«ČÜŅŗ×ŖŅʵ½ČŻĮæĘæÖŠ
B. ŌŚŹ¹ÓĆČŻĮæĘæĒ°±ŲŠė¼ģ²éČŻĮæĘæŹĒ·ńĶźŗĆŅŌ¼°ĘæČū“¦ŹĒ·ńĀ©Ė®
C. ¶ØČŻŹ±£¬Čō¼ÓĖ®³¬¹żæĢ¶ČĻߣ¬æÉÓĆ½ŗĶ·µĪ¹ÜŠ”ŠÄĪü³ö¶ąÓą²æ·Ö
D. ¶ØČŻŹ±£¬ČōŃöŹÓ£¬ŌņĖłÅäČÜŅŗµÄÅØ¶Č½«Ę«øß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅŠčŅŖ0.1 mol”¤L£1 NaOHČÜŅŗ450 mLŗĶ0.3 mol”¤L£1ĮņĖįČÜŅŗ480 mL”£øł¾ŻÕāĮ½ÖÖČÜŅŗµÄÅäÖĘĒéæö»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ČēĶ¼ŹĒŅŃĢį¹©ŅĒĘ÷£¬ÅäÖĘÉĻŹöČÜŅŗ¾łŠčÓƵ½µÄ²£Į§ŅĒĘ÷ŹĒ________£ØĢīŃ”Ļī£©”£
£Ø2£© ĻĀĮŠ²Ł×÷»įŹ¹ÅäÖʵÄNaOHČÜŅŗÅضČĘ«µĶµÄŹĒ__________”£
A ³ĘĮæNaOHĖłÓĆķĄĀėÉśŠā
B Ń”ÓƵÄČŻĮæĘæÄŚÓŠÉŁĮæÕōĮóĖ®
C ¶ØČŻŅ”ŌČŗó£¬ŅŗĆęĻĀ½µ£¬ÓÖ¼ÓĖ®ÖĮæĢ¶ČĻß
D ¶ØČŻŹ±ø©ŹÓæĢ¶ČĻß
£Ø3£©øł¾Ż¼ĘĖćÓĆĶŠÅĢĢģĘ½³ĘČ”NaOHµÄÖŹĮæĪŖ________g”£
£Ø4£©øł¾Ż¼ĘĖćµĆÖŖ£¬ĖłŠčÖŹĮæ·ÖŹżĪŖ98%”¢ĆܶČĪŖ1.84 g/cm3µÄÅØĮņĖįµÄĢå»żĪŖ__________mL£Ø¼ĘĖć±£ĮōŅ»Ī»Š”Źż£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ
A. 1.00molNaClÖŠŗ¬ÓŠNaCl·Ö×ÓŹżĪŖNA
B. 18gD2OŗĶ18gH2OÖŠŗ¬ÓŠµÄÖŹ×ÓŹż¾łĪŖ10NA
C. 1molFeøßĪĀĢõ¼žĻĀÓėĖ®Õō·“Ó¦£¬µē×Ó×ŖŅĘŹżĪŖ3NA
D. 12gŹÆÄ«Ļ©(µ„²ćŹÆÄ«)ÖŠŗ¬ÓŠĮłŌŖ»·µÄøöŹżĪŖ0.5NA
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com