
·ÖĪö ·¢Éś·“Ó¦£ŗZn+2HCl=ZnCl2+H2”ü£¬øł¾Żn=$\frac{m}{M}$¼ĘĖć13.0gZn·ŪµÄĪļÖŹµÄĮ棬ŌŁøł¾Ż·½³ĢŹ½¼ĘĖćÉś³ÉĒāĘųµÄĪļÖŹµÄĮæ£¬Éś³ÉĀČ»ÆŠæµÄĪļÖŹµÄĮ棬HClµÄĪļÖŹµÄĮ棬øł¾ŻV=nVm¼ĘĖćĒāĘųĢå»ż£¬øł¾ŻV=$\frac{n}{c}$¼ĘĖćŃĪĖįµÄĢå»ż£¬ĄūÓĆĖ«ĻßĒűķŹ¾µē×Ó×ŖŅĘ£¬ÓÉ·“Ó¦ĪļÖøĻņÉś³ÉĪļ£¬±ķŹ¾Ķ¬ÖÖŌŖĖŲÖ®¼äµē×ӵƏ§Ēéæö£¬²¢×¢Ć÷µē×Ó×ŖŅĘŹżÄ棬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗ£ŗ£Ø1£©2HCl+ZnØTZnCl2+H2”üÖŠŹ§µē×ÓµÄZnŌŖĖŲ»ÆŗĻ¼ŪÉżøߣ¬µĆµē×ÓµÄHŌŖĖŲ»ÆŗĻ¼Ū½µµĶ£¬ZnĪŖ»¹Ō¼Į£¬HClĪŖŃõ»Æ¼Į£¬»ÆŗĻ¼Ū½µµĶŹżÄæ=»ÆŗĻ¼ŪÉżøߏżÄæ=×ŖŅʵĵē×ÓŹżÄæ=2£¬µē×Ó×ŖŅĘĒéæöČēĻĀ£ŗ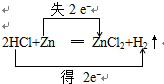 £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£»
£Ø2£©ÓÉ2HCl+ZnØTZnCl2+H2”üZnĪŖ»¹Ō¼Į£¬H+ĪŖŃõ»Æ¼Į£¬Éś³ÉZn2+ĪŖŃõ»Æ²śĪļ£¬ĖłŅŌŃõ»Æ¼ĮµÄŃõ»ÆŠŌ“óÓŚŃõ»Æ²śĪļµÄŃõ»ÆŠŌ£¬ŌņH+Ńõ»ÆŠŌ“óÓŚZn2+£¬“š£ŗH+Ńõ»ÆŠŌ“óÓŚZn2+£»
£Ø3-5£©ŠæµÄĦ¶ūÖŹĮæŹĒ65g/mol£¬ĖłŅŌŠæµÄĪļÖŹµÄĮæŹĒ13.0g”Ā65g/mol=0.2mol£¬
Zn+2 HCl=ZnCl2 +H2ӟ
1 2 1 1
0.2mol n£ØHCl£© n£ØZnCl2£© n£ØH2£©
Ōņn£ØHCl£©=$\frac{0.2mol”Į2}{1}$=0.4mol
n£ØZnCl2£©=n£ØH2£©=$\frac{0.2mol”Į1}{1}$=0.2mol
Ņņ“ĖŃĪĖįµÄĢå»żÖĮÉŁŹĒ0.4mol”Ā2mol/L=0.2L
Éś³ÉĀČ»ÆŠæŗĶĒāĘų¶¼ŹĒ0.2mol£¬
ĘäÖŠĒāĘųŌŚ±ź×¼×“æöĻĀµÄĢå»żŹĒ£ŗ0.2mol”Į22.4L/mol=4.48L£¬
“š£ŗ£Ø3£©ŃĪĖįµÄĢå»żÖĮÉŁŹĒ0.2L£¬£Ø4£©Éś³ÉĀČ»ÆŠæŹĒ0.2mol£¬£Ø5£©Éś³ÉĒāĘųŌŚ±ź×¼×“æöĻĀµÄĢå»żŹĒ4.48L£»
£Ø6£©ÓÉ £¬Ōņ0.2molZn²ĪÓė·“Ó¦×ŖŅʵĵē×ÓµÄøöŹżĪŖ2”Į0.2mol=0.4mol£¬“š£ŗ·“Ó¦ÖŠ×ŖŅʵĵē×ÓµÄøöŹżĪŖ0.4mol£®
£¬Ōņ0.2molZn²ĪÓė·“Ó¦×ŖŅʵĵē×ÓµÄøöŹżĪŖ2”Į0.2mol=0.4mol£¬“š£ŗ·“Ó¦ÖŠ×ŖŅʵĵē×ÓµÄøöŹżĪŖ0.4mol£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄĮæÓŠ¹Ų¼ĘĖć”¢»Æѧ·½³ĢŹ½¼ĘĖćŅŌ¼°µē×Ó×ŖŅʱķŹ¾·½·ØµÄ漲飬±Č½Ļ»ł“”£¬×¢Ņā¶Ō»ł“”ÖŖŹ¶µÄĄķ½āÕĘĪÕ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ²Ł ×÷ | ĻÖ Ļó | ½į ĀŪ |
| A | ĻņÕįĢĒÖŠ¼ÓČėÅØĮņĖį | ÕįĢĒ±ä³ÉŹčĖɶąæ×µÄŗ£Ćą×“Ģ棬²¢·Å³öÓŠŲŻ¼¤ŠŌĘųĪ¶µÄĘųĢå | ÅØĮņĖį¾ßÓŠĶŃĖ®ŠŌŗĶĒæŃõ»ÆŠŌ |
| B | ĻņŹ¢ÓŠH2O2ČÜŅŗµÄŹŌ¹ÜÖŠ¼ÓČė¼øµĪĖį»ÆµÄĮņĖįŃĒĢśČÜŅŗ | ČÜŅŗ±ä³É×Ų»ĘÉ«£¬Ņ»¶ĪŹ±¼äŗó£¬ČÜŅŗÖŠ³öĻÖĘųÅŻ£¬ĖęŗóÓŠŗģŗÖÉ«³ĮµķÉś³É | Fe2+“ß»ÆH2O2·Ö½ā²śÉśO2£»H2O2·Ö½ā·“Ó¦·ÅČČ£¬“Ł½ųFe3+µÄĖ®½āĘ½ŗāÕżĻņŅĘ¶Æ |
| C | ĀĮʬĻČÓĆÉ°Ö½“ņÄ„£¬ŌŁ¼ÓČė µ½ÅØĻõĖįÖŠ | ĪŽĆ÷ĻŌĻÖĻó | ÅØĻõĖį¾ßÓŠĒæŃõ»ÆŠŌ£¬³£ĪĀĻĀ£¬ĀĮ±»ÅØĻõĖį¶Ū»Æ |
| D | ĻņµČÅØ¶ČµÄKC1”¢KI»ģŗĻŅŗÖŠÖšµĪĀś¼ÓAgNO3ČÜŅŗ | ĻČ³öĻÖ»ĘÉ«³Įµķ | Ksp£ØAgCl£©£¾Ksp £ØAgI£© |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 °“ČēĶ¼×°ÖĆ½ųŠŠŹµŃ飬ĻĀĮŠĶʶĻÕżČ·µÄŹĒ£Ø””””£©
°“ČēĶ¼×°ÖĆ½ųŠŠŹµŃ飬ĻĀĮŠĶʶĻÕżČ·µÄŹĒ£Ø””””£©| Ń”Ļī | IÖŠŹŌ¼Į | IIÖŠŹŌ¼Į¼°ĻÖĻó | ĶʶĻ |
| A | ĀČ»Æļ§ | ·ÓĢŖČÜŅŗ²»±äŗģÉ« | ĀČ»Æļ§ĪČ¶Ø |
| B | ĮņĖįŃĒĢś | Ę·ŗģČÜŅŗĶŹÉ« | FeSO4·Ö½āÉś³ÉFeOŗĶSO2 |
| C | ĶæÓŠŹÆĄÆÓĶµÄĖé“Éʬ | ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ« | ŹÆĄÆÓĶ·¢ÉśĮĖ»Æѧ±ä»Æ |
| D | Ģś·ŪÓėĖ®ÕōĘų | ·ŹŌķĖ®Ć°ÅŻ | Ģś·ŪÓėĖ®ÕōĘų·¢ÉśĮĖ·“Ó¦ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | ||
| C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ü | B£® | ¢Ś¢Ū¢Ż | C£® | ¢Ū¢Ž¢ß | D£® | ¢Ż¢Ž¢ß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ü | B£® | ¢Ū¢Ü¢Ž¢ß¢ą¢į | C£® | ¢Ł¢Ū¢Ż¢ß¢ą¢į | D£® | ¢Ł¢Ū¢Ś¢Ü¢Ž¢ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ca£ØOH£©2ØTCa2++2OH- | B£® | KNO3ØTK++NO3- | ||
| C£® | H2SO4ØT2H++SO42- | D£® | Na2SO3ØTNa2++SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĢģČ»ĘųµÄÖ÷ŅŖ³É·ÖĪŖCH4 | |
| B£® | ŅŅĻ©ÓėäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗæÉ·¢Éś¼Ó³É·“Ó¦ | |
| C£® | CH4µÄ¶žĀČ“śĪļÖ»ÓŠŅ»ÖÖ£¬“ĖŹĀŹµæÉĖµĆ÷CH4ĪŖÕżĖÄĆęĢå½į¹¹ | |
| D£® | ³żČ„¼×ĶéĘųĢåÖŠµÄŅŅĻ©æÉŅŌ½«»ģŗĻĘųĢåĶعżŹ¢ÓŠ×ćĮæĖįŠŌøßĆĢĖį¼ŲČÜŅŗµÄĻ“ĘųĘæ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com