
| A. | c(H+)<c(OH-)<c(CH3COO-)<c(Na+) | B. | c(H+)<c(OH-)<c(Na+)<c(CH3COO-) | ||
| C. | c(H+)<c(CH3COO-)<c(OH-)<c(Na+) | D. | c(OH-)<c(CH3COO-)<c(H+)<c(Na+) |
分析 醋酸钠是强碱弱酸盐,醋酸根离子水解导致溶液呈碱性,但其水解程度较小,溶液中存在电荷守恒,结合电荷守恒分析解答.
解答 解:醋酸钠是强碱弱酸盐,醋酸根离子水解导致溶液呈碱性,则c(H+)<c(OH-),但其水解程度较小,所以c(OH-)<c(CH3COO-),溶液中存在电荷守恒c(OH-)+c(CH3COO-)=c(H+)+c(Na+),则c(CH3COO-)<c(Na+),所以离子浓度大小顺序是c(H+)<c(OH-)<c(CH3COO-)<c(Na+),故选A.
点评 本题考查离子浓度大小比较,为高频考点,侧重考查学生分析判断能力,明确溶液中溶质性质是解本题关键,注意:不是双水解的盐类水解较微弱,所以溶液的酸碱性较弱,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:实验题
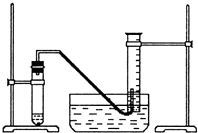 某学生利用锌与稀硫酸反应产生的氢气的体积,粗略测定锌的摩尔质量(设Wg锌片全部反应,产生气体的体积折算成标准状况时不超过50mL).实验装置如下:
某学生利用锌与稀硫酸反应产生的氢气的体积,粗略测定锌的摩尔质量(设Wg锌片全部反应,产生气体的体积折算成标准状况时不超过50mL).实验装置如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
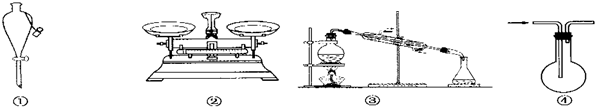
| A. | 仪器①可用于乙醇与水分离提纯 | |
| B. | 仪器②可用于称取5.85 g氯化钠固体 | |
| C. | 装置③的烧瓶中应加沸石,以防暴沸 | |
| D. | 装置④从箭头方向进气,用排空气法可收集H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气具有漂白性,可作漂白剂 | |
| B. | Fe2O3是一种红棕色粉末,常用作红色油漆 | |
| C. | Na2O2具有强氧化性,常用作供氧剂 | |
| D. | FeCl3能水解,可用于腐蚀印刷铜制电路板 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
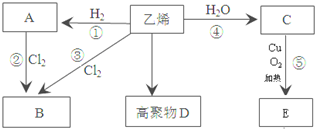
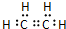 ,C中所含官能团的名称羟基;
,C中所含官能团的名称羟基;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50(b-2a) | B. | (b-2a) | C. | 50(b-a) | D. | 10(b-2a) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去AlCl3溶液中的FeCl3杂质的方法:先加入足量浓氨水,过滤,再加入过量盐酸,得到纯净AlCl3溶液 | |
| B. | 可以用金属钠和MgCl2溶液反应置换金属Mg;可以通过化合反应制备Fe(OH)3 | |
| C. | 对某溶液进行焰色反应,火焰呈黄色,则证明该溶液中含有钠盐,可能有钾盐 | |
| D. | 配制氯化铁溶液时,将氯化铁固体溶解在较浓的盐酸中再加水稀释 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com