
| A. | 溴水 | B. | 硫酸锌 | C. | 硝酸钠 | D. | 氯化铜 |
分析 铁屑溶于盐酸后,溶液中主要是H+、Cl-、Fe2+,若要将Fe2+变为Fe3+,需要强氧化性物质,据此解答.
解答 解:铁屑溶于盐酸后,溶液中主要是H+、Cl-、Fe2+,若要将Fe2+变为Fe3+,需要强氧化性物质.
A、溴水具有强的氧化性,能够氧化二价铁离子生成三价铁离子,故A正确;
B、硫酸锌中的锌离子和硫酸根均无强氧化性,不能将亚铁离子氧化,故B错误;
C、硝酸根离子在酸性环境下具有强的氧化性,能够将Fe2+氧化为Fe3+,故C正确;
D、Cu2+无的氧化性不足以将将Fe2+氧化为Fe3+,而氯离子无氧化性,故D错误.
故选AC.
点评 本题考查铁的化学性质,侧重氧化还原反应的考查,把握物质或离子的性质为解答的关键,注意硝酸根离子在酸性环境下具有强的氧化性,题目难度不大.


科目:高中化学 来源: 题型:解答题
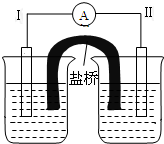 根据反应Fe+Fe2(SO4)3=3FeSO4设计的双液原电池如图所示.
根据反应Fe+Fe2(SO4)3=3FeSO4设计的双液原电池如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 不纯物质 | 除杂试剂 | 分离方法 |
| ① | 苯(苯酚) | ||
| ② | 酒精(水) | ||
| ③ | 溴苯(Br2) | ||
| ④ | 乙烯(SO2) | ||
| ⑤ | 乙酸乙酯(乙酸) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18H2O含有的氢原子数目为NA | |
| B. | 1molFe与足量盐酸反应失去的电子数为3NA | |
| C. | 标准状况下,22.4L等物质的量的CO2和O2混合气体中含有氧原子数为2NA | |
| D. | 2mol•L-1NaCl溶液中含有Na+个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 压强(Pa) | 4×105 | 6×105 | 10×105 | 20×105 |
| D的浓度(mol/L) | 0.085 | 0.126 | 0.200 | 0.440 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解质AgNO3溶液的浓度变为0.08mol/L | |
| B. | 阳极上产生112mLO2(标况) | |
| C. | 转移1.204×1022个电子 | |
| D. | 反应中有0.01mol的Ag被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com