
下列反应中,水作为还原剂的是
A.2F2+2H2O=4HF+O2 B. NaOH+HCl=NaCl+H2O
C. 2Na+2H2O=2Na++2OH-+H2↑ D. Cl2+H2O=HCl=HCl+HClO
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列实验操作中正确的是
A.蒸馏操作时,应向蒸馏液体中加入几块沸石,以防止暴沸
B.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
C.分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出
D.萃取操作时,可以选用CCl4或酒精作为萃取剂从溴水中萃取溴
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸(H2C2O4)是一种重要的有机化工原料。为探究草酸的制取和草酸的性质,进行如下实验。
实验Ⅰ:实验室用硝酸氧化淀粉水解液法制备草酸,装置如下图所示
①一定量的淀粉水解液加入三颈烧瓶中
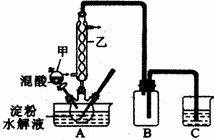
②控制反应温度55-60℃,边搅拌边缓慢滴加一定量的混合酸(65%的HNO3与98%的H2SO4的质量比2︰1.25)
③反应3小时,冷却,抽滤后再重结晶得到草酸晶体
硝酸氧化淀粉水解液的反应为:
C6H12O6+12HNO3 3H2C2O4+9NO2↑+3NO↑+9H2O
3H2C2O4+9NO2↑+3NO↑+9H2O
(1)上图实验装置中仪器乙的名称为:________________________。
装置B的作用是 。
(2)检验淀粉是否水解完全的方法:______________________________________________。[
实验Ⅱ:探究草酸与酸性高锰酸钾的反应
(3)向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,写出上述反应的离子方程式:____________________________________________________。
(4)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,溶液褪色总是先慢后快。为探究其原因,同学们做了如下对比实验;

由此你认为溶液褪色总是先慢后快的原因是_________________________________________。
(5)草酸亚铁在工业中有重要作用,草酸可以制备草酸亚铁,步骤如下:
称取FeSO4·7H2O 固体于小烧杯中,加入水和少量稀H2SO4溶液酸化,加热溶解。向此溶液中加入一定量的H2C2O4溶液,将混合溶液加热至沸,不断搅拌,以免暴沸,待有黄色沉淀析出并沉淀后,静置。倾出上清液,再加入少量水,并加热,过滤,充分洗涤沉淀,过滤,用丙酮洗涤固体两次并晾干。
①生成的草酸亚铁需充分洗涤沉淀,检验是否洗涤完全的方法是 。
②用丙酮洗涤固体两次的目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将2mol H2和1mol CO2充入体积为10L的恒容密闭容器中,在一定条件下发生反应:
①CO2(g) + H2(g) CO(g) + H2O(g) △H1=+41.2kJ·moL-1;
CO(g) + H2O(g) △H1=+41.2kJ·moL-1;
②CO2(g) + 3H2(g) CH3OH(g) + H2O(g) △H2=-49kJ·moL-1。
CH3OH(g) + H2O(g) △H2=-49kJ·moL-1。
反应100min后达到平衡,测得下表数据:
| 温度 | 转化率(%) | 物质的量(mol) | ||
| H2 | CO2 | CH3OH | CO | |
| 240℃ | 10 | 0.05 | 0.05 |
下列说法正确的是
A.升高温度,反应①的平衡常数减小
B.升高温度,CH3OH的含量提高
C.H2转化率为10%
D.100min内,反应②的速率为v(CO2)=0.0001 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语表达正确的是

A.Cl-的结构示意图:
|
|
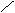
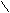 H H
H H

 C. CH4Si的结构式: C—Si
C. CH4Si的结构式: C—Si
H H
D. 质量数为137的钡原子:
查看答案和解析>>
科目:高中化学 来源: 题型:
只用一种试剂就可区别Na2SO4、AlCl3、NH4Cl、MgSO4 四种溶液。这种试剂是
A. HCl B. BaCl2 C. AgNO3 D. NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
在pH=1和pH=14的无色溶液中,都能大量共存的离子组是 ( )
A .Cu2+、Cl-、Mg2+、NO3- B. K+、Cl-、Na+、SO42-
C. SO32-、Na+、NO3-、Al3+ D. HCO3-、NH4+、Ag+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
在某温度下,可逆反应mA(g)+nB(g)  pC(g)+qD(g)的平衡常数为K,下列说法正确的是
pC(g)+qD(g)的平衡常数为K,下列说法正确的是
A.增加A的量,平衡正向移动,达到新平衡时K值增大
B.升高温度,K值增大
C.K越大,说明该反应的进行程度越大,转化率越高
D.该反应的K=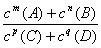
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com