
6.4 g铜与过量的硝酸(8 mol·L-1 60 mL)充分反应后,硝酸的还原产物有NO、NO2,反应后溶液中含H+为n mol,此时溶液中含NO3-的物质的量为( )
A.0.28 mol B.0.31 mol
C.(n+0.2) mol D.(n+0.4)mol
科目:高中化学 来源: 题型:
3,5二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:
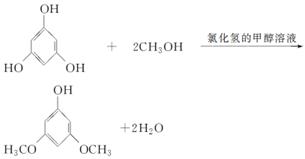
甲醇、乙醚和3,5二甲氧基苯酚的部分物理性质见下表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20 ℃) /g·cm-3 | 溶解性 |
| 甲醇 | 64.7 | — | 0.791 5 | 易溶于水 |
| 乙醚 | 34.5 | — | 0.713 8 | 微溶于水 |
| 3,5二甲氧基苯酚 | — | 33~36 | — | 易溶于甲醇、乙醚,微溶于水 |
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。①分离出甲醇的操作是________________。②萃取用到的分液漏斗使用前需________并洗净,分液时有机层在分液漏斗的________(填“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是________;用饱和食盐水洗涤的目的是_______________。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是________(填字母)。
a.蒸馏除去乙醚 b.重结晶
c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤。为了防止倒吸,减压过滤完成后应先________,再________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某固体物质X与稀盐酸反应生成溶液Y,Y与过量氢氧化钠溶液反应得白色沉淀Z,经过滤后,将沉淀物Z加热灼烧又得到X。则X可能是 ( )
A.Fe2O3 B.Al2O3 C.FeO D.MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
中学常见的某反应的化学方程式为A+B―→C+D+H2O(未配平,反应条件略去)。请回答下列有关问题:
(1)若A是铁,B是稀硝酸(过量),且A可溶于C溶液中。则A与B反应的离子方程式为________________________________________________________________________。
(2)若C、D均为气体,且都能使澄清石灰水变浑浊,则上述反应的化学方程式为________________________________________________________________________。
(3)若C是无色刺激性气味的气体,其水溶液呈弱碱性,C能发生催化氧化反应。写出该反应的化学方程式_______________________________________________________
________________________________________________________________________。
(4)若D为氯碱工业的主要原料,C是造成温室效应的主要气体之一,则上述反应的化学方程式
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
设C+CO2 2CO ∆H>0,反应速率为v1,N2 +3H2 2NH3 ∆H<0,反应速率为v2,对于上述反应,当温度升高时,v1和v2的变化情况为
A.同时增大 B.同时减小 C.增大,减小 D.减小,增大
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H-H键键能(断裂时吸收或生成时释放的能量)为436 kJ·mol-1,H-N键键能为391 kJ·mol-1,根据热化学方程式:
N2(g) +3H2(g) =2NH3(g) ΔH=-92.4 kJ·mol-1。则N≡N键的键能是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲是一种盐,由A、B、C、D、E五种元素组成,其中四种是短周期元素。甲溶于水后可电离出三种离子,其中含有由A、B形成的10电子阳离子。A元素原子核内质子数比E的少1,D、E处于同主族。
用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中滴入KSCN溶液,无现象,再滴入氯水,溶液呈红色;
③取少量甲溶液于试管中加入适量NaOH溶液,加热;
④取少量甲溶液于试管中,向其中加入稀盐酸,再加入BaCl2溶液,出现白色沉淀。
回答下列问题:
(1)C的元素符号是 ,D在周期表中的位置 。
(2)用离子方程式表示实验②中现象的原因: 。
(3)实验③中出现的现象是 。
(4)甲中阳离子与阴离子物质的量之比为3:2,则甲的化学式为 。
(5)某同学以氨气和二氧化碳为原料制备碳酸氢铵。合理的方案是
A.先将二氧化碳通入水中,充分溶解后,再通入氨气。
B.先将氨气通入水中,充分溶解后,再通入二氧化碳。
检验产物中有NH4+的方法为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com