
 ,B的名称是1,2-二溴环己烷.
,B的名称是1,2-二溴环己烷.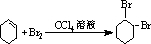 .
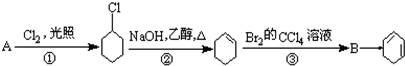
. 分析 由合成流程可知,A为 ,①为取代反应生成
,①为取代反应生成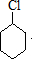 ,反应②为消去反应生成
,反应②为消去反应生成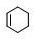 ,反应③为加成反应生成B为
,反应③为加成反应生成B为 ,最后发生消去反应生成环己二烯,以此来解答.
,最后发生消去反应生成环己二烯,以此来解答.
解答 解:由合成流程可知,A为 ,①为取代反应生成
,①为取代反应生成 ,反应②为消去反应生成
,反应②为消去反应生成 ,反应③为加成反应生成B为
,反应③为加成反应生成B为 ,最后发生消去反应生成环己二烯,
,最后发生消去反应生成环己二烯,
(1)A的结构简式是 ,B的名称是1,2-二溴环己烷,故答案为:
,B的名称是1,2-二溴环己烷,故答案为: ;1,2-二溴环己烷;
;1,2-二溴环己烷;
(2)由上述分析可知,②的反应类型是消去反应,故答案为:消去反应;
(3)反应③的化学方程式是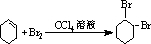 ,故答案为:
,故答案为: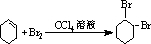 .
.
点评 本题考查有机物的合成,为高频考点,把握合成流程中官能团的变化、有机反应为解答的关键,侧重分析与应用能力的考查,注意卤代烃、烯烃的性质,题目难度不大.


科目:高中化学 来源: 题型:解答题
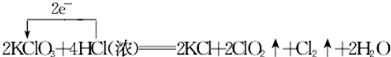 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
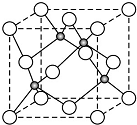 原子序数小于36的X、Y、Z、W四种元素,其中X是半径最小的元素,Y原子基态时成对电子数是其未成对电子总数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W原子4s原子轨道上有1个电子,M能层为全充满的饱和结构.回答下列问题:
原子序数小于36的X、Y、Z、W四种元素,其中X是半径最小的元素,Y原子基态时成对电子数是其未成对电子总数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W原子4s原子轨道上有1个电子,M能层为全充满的饱和结构.回答下列问题: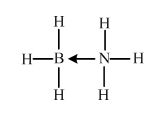 (必须标明配位键)
(必须标明配位键)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
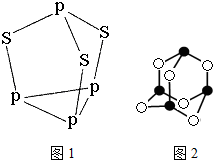 磷和砷元素形成的化合物在生活和生产中有重要的用途,回答下列问题.
磷和砷元素形成的化合物在生活和生产中有重要的用途,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaF 的水解产物是NaOH 和HF | B. | CaO2 的水解产物是Ca(OH)2 和H2O2 | ||
| C. | PCl3 的水解产物之一是PH3 | D. | Mg3N2水解产物是Mg(OH)2和NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
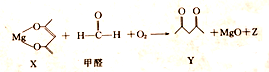
| A. | X 是还原剂 | B. | Y的分子式为C5H8O2 | ||
| C. | Z的摩尔质量为44g | D. | 除去1mol甲醛时,转移2mole- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com