
(1)求所得滤液中溶质的质量分数。
(2)求过滤后,所得滤渣的质量。
(20 ℃,NaCl的溶解度是36 g)
错因分析:没有注意到NaCl没有全部溶解而导致错误。
w(NaCl)=![]() ×100%=27.5%,
×100%=27.5%,
滤渣认为只有BaSO4 23.3 g。
正解:Na2SO4质量为:71 g×20%=14.2 g
Na2SO4 + BaCl2====BaSO4↓ + 2NaCl
142 208 233 117
14.2 g (20.8 g) (23.3 g) (11.7 g)
溶剂水的质量:71 g-14.2 g=56.8 g,能够溶解的NaCl质量为m,
100 g∶36 g====56.8 g∶m
m=20.4 g
NaCl总质量为:30.6 g-20.8 g+11.7 g=21.5 g>20.4 g,NaCl没有全部溶解,没有溶解的NaCl为:21.5 g-20.4 g=1.1 g,则所得滤液是NaCl的饱和溶液,该溶液溶质的质量分数为:
![]() ×100%=26.4%或
×100%=26.4%或![]() ×100%=26.4%,
×100%=26.4%,
滤渣是BaSO4和NaCl,质量为:23.3 g+1.1 g=24.4 g。
答案:(1)26.4% (2)24.4 g


科目:高中化学 来源: 题型:
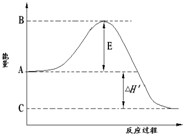 合成氨工业是极为重要的化学工业,当今对合成氨工业的研究仍然充满活力.其合成原理为:N2(g)+3H2(g)?2NH3(g);△H=-92.2kJ/mol.回答下列问题:
合成氨工业是极为重要的化学工业,当今对合成氨工业的研究仍然充满活力.其合成原理为:N2(g)+3H2(g)?2NH3(g);△H=-92.2kJ/mol.回答下列问题:| 1 |
| 3 |
| 10 | 20 | 30 | 60 | |
| 300 | 52.0 | 64.2 | 71.0 | 84.2 |
| 400 | 25.1 | 38.2 | 47.0 | 65.2 |
| 500 | 10.6 | 19.1 | 26.4 | 42.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com