
 NH4++OH-;实验室制备A的氢化物的化学方程式为Ca(OH)2+2NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O.
NH4++OH-;实验室制备A的氢化物的化学方程式为Ca(OH)2+2NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O.分析 A、B、C、D、E五种元素的原子序数依次增大,其中A、B、C、D为短周期元素,且只有A、D为非金属元素.A的氢化物溶于水得到的溶液能使酚酞溶液变红,则A为N元素;B、C、D的最高价氧化物对应水化物相互之间能够两两反应,是氢氧化铝、强碱、强酸之间的反应,则B为Na、C为Al,D为S或Cl,由于D原子最外层电子数是C原子最外层电子数的2倍,则D为S元素,B、E元素同主族,且原子序数相差8,则E为K.
解答 解:A、B、C、D、E五种元素的原子序数依次增大,其中A、B、C、D为短周期元素,且只有A、D为非金属元素.A的氢化物溶于水得到的溶液能使酚酞溶液变红,则A为N元素;B、C、D的最高价氧化物对应水化物相互之间能够两两反应,是氢氧化铝、强碱、强酸之间的反应,则B为Na、C为Al,D为S或Cl,由于D原子最外层电子数是C原子最外层电子数的2倍,则D为S元素,B、E元素同主族,且原子序数相差8,则E为K.
(1)E为K元素,在元素周期表中的位置:第四周期IA族,E的最高价氧化物对应水化物为KOH,与C的单质Al反应的化学方程式:2KOH+2Al+2 H2O=2 KAlO2+3 H2↑,
故答案为:第四周期IA族;2KOH+2Al+2 H2O=2 KAlO2+3 H2↑;
(2)A的氢化物为NH3,溶于水后的电离方程式为:NH3•H2O  NH4++OH-,实验室制备A的氢化物的化学方程式为:Ca(OH)2+2NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O,
NH4++OH-,实验室制备A的氢化物的化学方程式为:Ca(OH)2+2NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O,
故答案为:NH3•H2O  NH4++OH-;Ca(OH)2+2NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O;
NH4++OH-;Ca(OH)2+2NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O;
(3)B单质Na在空气中燃烧后的产物为Na2O2,存在的化学键类型有离子键、共价键,Na2O2和水反应的离子方程式:2 Na2O2+2H2O=4Na++4OH-+O2↑,
故答案为:Na2O2;离子键、共价键;2 Na2O2+2H2O=4Na++4OH-+O2↑.
点评 本题考查结构性质位置关系应用,侧重对化学用语的考查,推断元素是解题关键,注意对元素化合物性质的理解掌握.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | “另一种反应物”一定具有还原性 | B. | “另一种反应物”一定只具有氧化性 | ||
| C. | 2CuH+3Cl2 $\frac{\underline{\;点燃\;}}{\;}$2CuCl2+2HCl | D. | CuH既可作氧化剂也可作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W的最高价氧化物对应的水化物难溶于水 | |
| B. | 原子半径按X、Y、Z、R、W的顺序依次增大 | |
| C. | Z与Y形成的化合物是碱性氧化物 | |
| D. | WY2能与强碱溶液反应,但不能与任何酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属元素和非金属元素形成的化合物一定是离子化合物 | |
| B. | 18O2和18O3互为同素异形体,相同状况下其密度之比为2:3 | |
| C. | 过渡元素都是副族元素 | |
| D. | 同主族元素的原子最外层电子数相同,化学性质也相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、C两种元素组成的化合物CA为共价化合物 | |
| B. | B元素可形成多种同素异形体 | |
| C. | C元素存在多种核素 | |
| D. | D的氧化物是两性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )广泛存在于可可、咖啡、草莓等物质中,可用作食物和日化用品的香精.已知:X的产量可以用来衡量一个国家的石油化工发展水平,工业上可用X和甲苯人工合成乙酸苯甲酯.其合成路线如下:
)广泛存在于可可、咖啡、草莓等物质中,可用作食物和日化用品的香精.已知:X的产量可以用来衡量一个国家的石油化工发展水平,工业上可用X和甲苯人工合成乙酸苯甲酯.其合成路线如下:
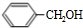 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$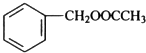 +H2O.
+H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ba2+、Cl-、SO42- | B. | Fe2+、H+、S2-、ClO- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、OH-、NO3-、HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
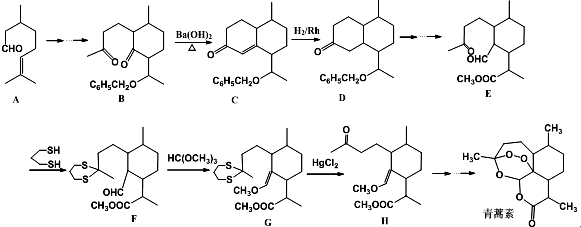
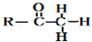 +
+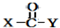 $\stackrel{OH-}{→}$
$\stackrel{OH-}{→}$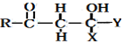
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com