
 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | |
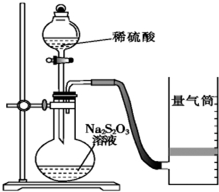
分析 Ⅰ.(1)从实验装置可知,本实验是通过测量在一个时间段内所收集到的气体的体积来测定反应速率,所以先要检查装置的气密性,实验仪器还需要秒表;
(2)SO2易溶于水,导致所测得的SO2的体积偏小;
(3)根据反应S2O32-+2H+═H2O+S↓+SO2↑可知,可以通过测定生成的单质硫的质量或实时测定溶液中氢离子浓度来求出H+的物质的量的改变量,从而求出反应速率;
Ⅱ.(4)为了探究反应物浓度对化学反应速率的影响,则除了Na2S2O3溶液的浓度不同外,应保持其他影响因素一致;淀粉作为显色剂,检验碘的存在,可根据颜色的变化判断反应的快慢;由于在三个实验中Na2S2O3溶液的浓度①>②>③,据此分析化学反应速率和反应所需时间t的大小.
解答 解:Ⅰ.(1)从实验装置可知,本实验是通过测量在一个时间段内所收集到的气体的体积来测定反应速率,所以先要检查装置的气密性,实验仪器还需要秒表,
故答案为:检查装置的气密性;秒表;
(2)SO2易溶于水,导致所测得的SO2的体积偏小,则据此计算出的△n(H+)和△C(H+)以及V(H+)会变小,
故答案为:SO2会部分溶于水,导致所测得SO2体积偏小;
(3)根据反应S2O32-++2H+═H2O+S↓+SO2↑可知,可以通过测定一段时间段内生成的单质硫的质量或实时测定溶液中氢离子浓度来求出H+的物质的量的改变量,
故答案为:测定一段时间内生成硫单质的质量或测定一定时间内溶液H+浓度的变化;
Ⅱ.(4)为了探究反应物浓度对化学反应速率的影响,则除了Na2S2O3溶液的浓度不同外,应保持其他影响因素一致,即应使溶液体积均为16mL,故Vx=4mL;淀粉作为显色剂,检验碘的存在,可根据颜色的变化判断反应的快慢;由于在三个实验中Na2S2O3溶液的体积①>②>③,而混合后溶液体积相同,故混合后Na2S2O3浓度①>②>③,可知化学反应速率①>②>③,反应所需时间T的大小t1<t2<t3,
故答案为:探究反应物浓度(Na2S2O3)对化学反应速率的影响;作为显色剂,检验I2的存在;4;t1<t2<t3.
点评 本题主要考查探究影响化学反应速率因素的条件,注意实验的基本操作,对化学反应速率的理解,在实验中常用控制变量法探究,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 增大压强,则反应的②K不变,反应①和③的K减小 | |
| B. | 500℃时,2NH3 (g)+2O2 (g)?N2O (g)+3H2O (g) K=2.2×1028 | |
| C. | 500℃时,N2 (g)+O2 (g)=2NO (g)△H=+181 kJ•mol-1 | |
| D. | 500℃时,2 mol NH3与2.5 mol O2混合发生反应①,可放出热量453.6 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
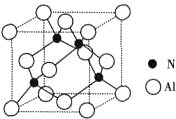 由N元素和Al元素形成的化合物的晶胞如图所示,已知N原子位于晶胞体对角线的$\frac{1}{4}$处.假设该化合物的密度为ρg•cm-3,则晶胞中最近的两个N原子之间的距离为$\frac{\sqrt{2}}{2}$$\root{3}{\frac{164}{{N}_{A}ρ}}$.
由N元素和Al元素形成的化合物的晶胞如图所示,已知N原子位于晶胞体对角线的$\frac{1}{4}$处.假设该化合物的密度为ρg•cm-3,则晶胞中最近的两个N原子之间的距离为$\frac{\sqrt{2}}{2}$$\root{3}{\frac{164}{{N}_{A}ρ}}$.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
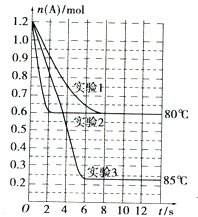 将1.2mol的A气体充入2L恒容密闭容器中发生反应:A(g)?2B(g).在三种不同条件下进行实验,A的物质的量随时间的变化如图所示.试回答下列问题:
将1.2mol的A气体充入2L恒容密闭容器中发生反应:A(g)?2B(g).在三种不同条件下进行实验,A的物质的量随时间的变化如图所示.试回答下列问题:| 实验编号 及其目的 | V(容积)/L | t/℃ | n(A起始)/mol | n(B起始)/mol | 催化剂的质量/g | 催化剂的表面积/m2•g-1[来源:Z.xx.k.Com] |
| 实验1 参照对比实验 | 2 | 80 | 1.2 | 0 | a | b |
| 实验4:催化剂的表面积对反应速率的影响 | | | | | | |
| 实验5目的: | 1 | | | | | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴入KMnO4溶液的次序 | KMnO4溶液紫色褪去所需的时间 |
| 先滴入第1滴 | 60s |
| 褪色后,再滴入第2滴 | 15s |
| 褪色后,再滴入第3滴 | 3s |
| 褪色后,再滴入第4滴 | 1s |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
 通过电解饱和食盐水得到的氢氧化钠固体样品常含有氯化钠杂质.来来同学利用中和滴定原理测定氢氧化钠的质量分数.步骤为:
通过电解饱和食盐水得到的氢氧化钠固体样品常含有氯化钠杂质.来来同学利用中和滴定原理测定氢氧化钠的质量分数.步骤为:| 实验序号 | 待测样品溶液体积(mL) | 滴定管读数 | 消耗标准盐酸溶液的体积(mL) | |
| 初读数 | 末读数 | |||
| 1 | 20.00 | 0.00 | 19.95 | 19.95 |
| 2 | 20.00 | 0.05 | 19.90mL | 19.85mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、NO3-、OH-、Cl- | B. | H+、Ba2+、Ag+、Cl- | ||
| C. | Fe2+、Fe3+、Na+、NO3- | D. | Ca2+、H+、Cl-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.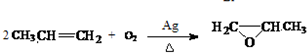 .
. .
.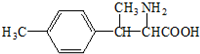 .
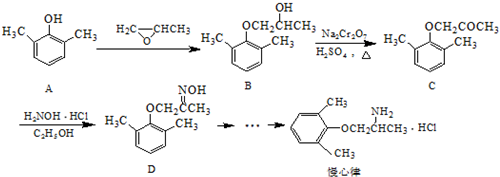
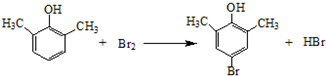
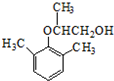
.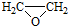 ).写出以邻甲基苯酚 (
).写出以邻甲基苯酚 (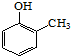 )和乙醇为原料制备
)和乙醇为原料制备 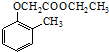 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2.
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com