
| 选项 | 实验目的 | 实验操作 |
| A | 配制CuSO4溶液 | 将硫酸铜晶体溶于热水中,然后稀释 |
| B | 除去试管内壁的银镜 | 加入浓氨水浸泡,再用蒸馏水洗涤 |
| C | 提纯含少量乙酸的乙醇(乙醇沸点78.5℃) | 加入生石灰后进行蒸馏,收集78.5℃馏分 |
| D | 证明HClO为弱酸 | 用洁净的玻璃棒蘸取NaClO溶液在pH试纸上,待试纸变色后与标准比色对照 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.热水中促进了铜离子的水解,应该在水中加入少量稀硫酸;
B.银单质不与氨水反应,可以用稀硝酸;
C.先将乙酸转化成沸点较高的盐,然后通过蒸馏分离出乙醇;
D.次氯酸具有漂白性,不能用pH试纸沉淀其pH.
解答 解:A.由于铜离子水解,则配制硫酸铜溶液时应该加入少量稀硫酸,以便抑制铜离子的水解,故A错误;
B.氨水不与银反应,除去试管内壁的银镜通常用稀硝酸,故B错误;
C.提纯含少量乙酸的乙醇时,加入生石灰将乙酸转化成乙酸钙,乙酸钙的沸点较高,然后进行蒸馏,收集78.5℃馏分可分离出乙醇,故C正确;
D.HClO具有强氧化性,能够漂白试纸,所以不能用pH试纸测定其pH,可选用pH计,故D错误;
故选C.
点评 本题考查了化学实验方案的评价,题目难度中等,涉及盐的水解原理、物质分离与提纯、次氯酸的漂白性等知识,明确常见化学实验基本操作方法为解答关键,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| 实验① | 实验② | 实验③ |
| 将铁钉放入硫酸 铜溶液中 | 向硫酸亚铁溶液中 滴入几滴浓硝酸 | 将铜丝放入 氯化铁溶液中 |
| A. | 可以用实验①的方法冶炼铜 | |
| B. | 实验②中Fe2+既显氧化性又显还原性 | |
| C. | 实验③中发生置换反应 | |
| D. | 上述实验证明氧化性:Fe3+>Fe2+>Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +4Mg+8CH3OH→
+4Mg+8CH3OH→ +4Mg(OCH3)2+4H2O
+4Mg(OCH3)2+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF的沸点高于HCl | B. | 金刚石的熔点比晶体硅高 | ||
| C. | 稀有气体一般很难发生化学反应 | D. | 常温下单质溴呈液态、碘呈固态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 太原市自2016年11月1日零时起,将汽车用油全部更换为”国V标准”车用燃料,进而 改善太原市空气质量.下列物质中,不会造成空气污染的是( )
太原市自2016年11月1日零时起,将汽车用油全部更换为”国V标准”车用燃料,进而 改善太原市空气质量.下列物质中,不会造成空气污染的是( )| A. | NO | B. | SO2 | C. | CO2 | D. | 粉尘 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
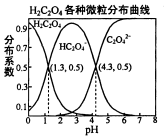 常温下,0.1mol/L的H2C2O4溶液中H2C2O4、HC2O4-、C2O42-三者中所占物质的量分数〔分布系数)随PH变化的关系如图所示.下列表述不正确的是( )
常温下,0.1mol/L的H2C2O4溶液中H2C2O4、HC2O4-、C2O42-三者中所占物质的量分数〔分布系数)随PH变化的关系如图所示.下列表述不正确的是( )| A. | HC2O4-?H++C2O42-,K=1×10-4.3 | |
| B. | 将等物质的量的NaHC2O4、Na2C2O4溶于水中,所得溶液PH恰好为4.3 | |
| C. | 常温下HF的KB=1×10--3.45,将少量H2C2O4溶液加入到足量NaF溶液中,发生的反应为:H2C2O4+F-=HF+HC2O4- | |
| D. | 在0.1mol/LNaHC2O4溶液中,各离子浓度大小关系为:c(Na+)>c(HC2O4-)>c(C2O42-)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 实验室用间二硝基苯通过催化加氢制备间硝基苯胺的实验步骤如下:
实验室用间二硝基苯通过催化加氢制备间硝基苯胺的实验步骤如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com