
【题目】下列实验能达到预期目的的是
编号 | 实验内容 | 实验目的 |
A | 向含有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
B | 室温下,用pH试纸分别测定浓度为18mol/L和0.1 mol/L H2SO4溶液的pH | 比较不同浓度H2SO4的酸性强弱 |
C | 配制FeCl2溶液时,先将FeCl2溶于适量浓盐酸中,再用蒸馏水稀释到所需浓度,最后在试剂瓶中加入少量铜粉 | 抑制Fe2+水解,并防止Fe2+被氧化 |
D | 向盛有1mL 0.01 mol/L | 证明在相同温度下的 Ksp(AgCl)>Ksp(AgI) |
A. A B. B C. C D. D
科目:高中化学 来源: 题型:
【题目】对于3Br2+6NaOH![]() 5NaBr+NaBrO3+3H2O的反应,下列说法中不正确的是( )
5NaBr+NaBrO3+3H2O的反应,下列说法中不正确的是( )
A. Br 2既是氧化剂,又是还原剂
B. 被氧化的溴原子与被还原的溴原子质量比是1:5
C. NaBr是氧化产物,NaBrO3是还原产物
D. 转移1mol电子时,消耗NaOH 1.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃,101kPa下,1gC8H28(辛烷)燃烧生成二氧化碳和液态水时放出48.4kJ热量.表示上述反应的热化学方程式正确的是
A. C8H28(l)+ ![]() O2(g)===8CO2(g)+9H2O(l) △H=-5517.6 KJ·mol—1
O2(g)===8CO2(g)+9H2O(l) △H=-5517.6 KJ·mol—1
B. C8H28(l)+ ![]() O2(g)===8CO2(g)+9H2O(l) △H=-48.4 KJ·mol—1
O2(g)===8CO2(g)+9H2O(l) △H=-48.4 KJ·mol—1
C. C8H28(l)+ ![]() O2(g)===8CO2(g)+9H2O(l) △H=+5517.6 KJ·mol—1
O2(g)===8CO2(g)+9H2O(l) △H=+5517.6 KJ·mol—1
D. C8H28(l)+ ![]() O2(g)===8CO2(g)+9H2O(l) △H=+48.4 KJ·mol—1
O2(g)===8CO2(g)+9H2O(l) △H=+48.4 KJ·mol—1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是 ( )
A. 氢氧化钠溶液与稀醋酸反应:OH-+H+=H2O
B. 碳酸钙与足量稀硝酸反应:CaCO3+2H+=Ca2++H2O+CO2↑
C. 氯化铝溶液与过量氨水反应:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
D. 钠与水反应:Na+2H2O=Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示。常温下,B、E呈气态,其中B呈黄绿色。D是最常见的无色液体,E常用作制冷剂,F是一种不溶于水的碱,G是厨房中的常见调味品,H由两种元素组成,其摩尔质量为32 g·mol-1。

(1) E的电子式为____。
(2) H的化学式为____。
(3) 写出反应①的离子方程式:_________________。
(4) 写出反应②的化学方程式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列浓度关系正确的是( )
A. 0.1mol/L的NH4HSO4溶液中滴加0.1mol/L的Ba(OH)2溶液至沉淀刚好完全:c(NH4+)>c(OH-)>c(SO42-)>c(H+)
B. 若将CO2通入0.1mol/LNa2CO3溶液至溶液中性,则溶液中: 2c(CO32-)+c(HCO3-)=0.1mol/L
C. 0.1mol/L的NaOH溶液与0.2mol/L的HCN溶液等体积混合,所得溶液呈碱性:c(Na+)>c(CN-)>c(HCN)>c(OH-)>c(H+)
D. 向1L 1mol/L的KOH热溶液中通入一定量的Cl2,恰好完全反应生成氯酸钾、次氯酸钾和氯化钾的混合溶液:c(K+)+c(H+)=6c(ClO3-)+2c(ClO-)+c(HClO)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是丁烷裂解的实验流程:(提示:丁烷在一定条件下裂解的可能方程式为:C4H10![]() C2H6+C2H4, C4H10
C2H6+C2H4, C4H10![]() CH4+C3H6)
CH4+C3H6)
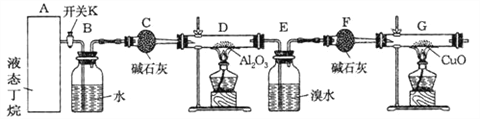
连接好装置后,需进行的实验操作有:
①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等…
(1)这三步操作的先后顺序依次是_______________________(填序号)
(2)写出甲烷与氧化铜反应的化学方程式______________________
(3)若对E装置中的混合物(溴水足量),再按以下流程实验:
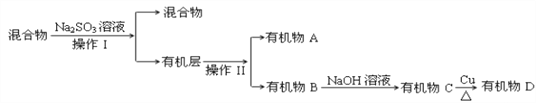
①分离操作Ⅰ和Ⅱ的名称分别是:Ⅰ________Ⅱ________,Na2SO3溶液的作用是(用离子方程式表示)________________________________________________________.
②已知B的碳原子数大于A的碳原子数,请写出B的结构简式_____________________.
(4)假定丁烷完全裂解,当(E+F)装置的总质量比反应前增加了0.7 g, G装置的质量减少了1.76 g,则丁烷的裂解产物中甲烷和乙烷的物质的量之比 n(CH4): n(C2H6)=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将赤铜矿(Cu2O)与辉铜矿(Cu2S)混合加热发生以下反应:2Cu2O+Cu2S![]() 6Cu+SO2↑,下列说法错误的是
6Cu+SO2↑,下列说法错误的是
A. 在Cu2O、Cu2S中Cu元素化合价都是+1价 B. 反应中Cu元素被氧化,S元素被还原
C. Cu2S在反应中既是氧化剂,又是还原剂 D. 每生成6.4gCu,反应中转移0.1mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下溶液的酸碱性对TiO2光催化燃料R降解反应的影响如图所示。下列判断正确的是

A.溶液酸性越强,R 的降解速率越小
B.R的起始浓度越小,降解速率越大[
C.在0~50 min之间,pH=2和PH=7时R的降解百分率相等
D.在20~25 min之间,pH=10 时R的平均降解速率为0.04 mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com