
分析 (1)原电池中,失电子发生氧化反应的电极是负极、得电子发生还原反应的电极是正极,根据电池反应式知,Ag失电子发生氧化反应、氢离子得电子发生还原反应,所以Ag是负极、不如Ag活泼的石墨作正极;
(2)负极上Ag溶解,生成的银离子和碘离子反应生成AgI黄色沉淀;
(3)根据Ag和转移电子之间的关系式计算转移电子物质的量,根据转移电子守恒计算生成氢气体积.
解答 解:(1)该反应方程式中,Ag元素化合价由0价变为+1价、H元素化合价由+1价变为0价,所以有电子转移,为氧化还原反应;原电池中,失电子发生氧化反应的电极是负极、得电子发生还原反应的电极是正极,根据电池反应式知,Ag失电子发生氧化反应、氢离子得电子发生还原反应,所以Ag是负极、不如Ag活泼的石墨作正极,
故答案为:氧化还原反应;Ag;
(2)负极上Ag溶解,生成的银离子和碘离子反应生成AgI黄色沉淀,所以看到的现象是:Ag电极逐渐溶解、负极附近有黄色沉淀生成,电极反应式为Ag-e-+I-=AgI↓,
故答案为:Ag电极逐渐溶解、负极附近有黄色沉淀生成;Ag-e-+I-=AgI↓;
(3)根据Ag和转移电子之间的关系式得转移电子物质的量=$\frac{5.4g}{108g/mol}×1$=0.05mol,根据转移电子守恒计算生成氢气体积=$\frac{0.05mol}{2}×22.4L/mol$=560mL,
故答案为:0.05;560.
点评 本题考查原电池设计,为高频考点,侧重考查学生分析判断及计算能力,明确原电池元素化合价变化与正负极的关系是解本题关键,难点是电极反应式的书写,题目难度不大.


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案科目:高中化学 来源: 题型:解答题
| 沸点/℃ | |
| SiHCl3 | 33.0 |
| SiCl4 | 57.6 |
| HCl | -84 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/×10-3 mol•L-1 | 1.00 | 0.45 | 0.25 | 0.15 | 0.10 | 0.10 |
| c(CO)/×10-3 mol•L-1 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
| A. | 2 s 内的平均反应速率υ(N2)=1.875×10-4 mol•L-1•s-1 | |
| B. | 在该温度下K=5 | |
| C. | 若将容积缩小为原来的一半,NO 转化率大于90% | |
| D. | 某时刻再充入0.1 mol NO,0.36 mol CO,重新达平衡后CO 浓度比原平衡大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | C | CO | C2H6 | C2H5OH |
| 燃烧热/KJ•mol-1 | 393.5 | 283 | 1559.8 | 1366.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
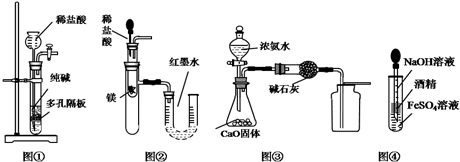
| A. | 用图①所示装置制取少量纯净的CO2气体 | |
| B. | 用图②所示装置验证镁和盐酸反应的热效应 | |
| C. | 用图③所示装置制取并收集干燥纯净的NH3 | |
| D. | 用图④装置制备Fe(OH)2并能保证较长时间观察到白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3mol | B. | 0.4mol | C. | 0.5mol | D. | 0.6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
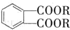 (代号DMP)是一种常用的酯类塑化剂,其蒸气对氢气的相对密度为97.工业上生产DMP的流程如图所示:
(代号DMP)是一种常用的酯类塑化剂,其蒸气对氢气的相对密度为97.工业上生产DMP的流程如图所示: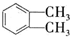 $→_{①光照}^{Cl_{2}}$[A]$\stackrel{②}{→}$[B]$→_{③△}^{Cu、O_{2}}$[C]$\stackrel{④}{→}$[D]$→_{⑤ROH/△}^{浓硫酸}$[DMP]
$→_{①光照}^{Cl_{2}}$[A]$\stackrel{②}{→}$[B]$→_{③△}^{Cu、O_{2}}$[C]$\stackrel{④}{→}$[D]$→_{⑤ROH/△}^{浓硫酸}$[DMP]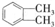 的名称1,2-二甲苯(或邻二甲苯),C中官能团的名称为醛基,DMP的分子式为C10H10O4.
的名称1,2-二甲苯(或邻二甲苯),C中官能团的名称为醛基,DMP的分子式为C10H10O4.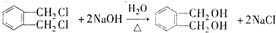 .
. .
.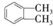 制备DMP的另一种途径:
制备DMP的另一种途径: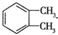 $→_{O_{2}①}^{催化剂、△}$
$→_{O_{2}①}^{催化剂、△}$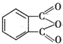 $→_{F②}^{适当条件}$[DMP]
$→_{F②}^{适当条件}$[DMP]查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com