
 ;
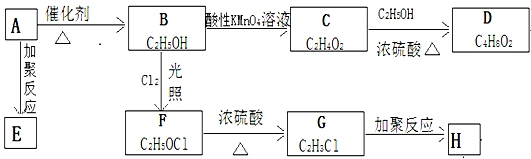
;分析 A既是一种重要的化工原料,也是一种水果催熟剂,则A为CH2=CH2,A和水反应生成B,B为CH3CH2OH,A发生加聚反应生成E,E为 ,B在光照条件下发生取代反应生成F,F为CH2ClCH2OH,F在浓硫酸作催化剂加热条件下发生消去反应生成G,G为CH2=CHCl,G发生加聚反应生成H,H为
,B在光照条件下发生取代反应生成F,F为CH2ClCH2OH,F在浓硫酸作催化剂加热条件下发生消去反应生成G,G为CH2=CHCl,G发生加聚反应生成H,H为 ;B被酸性高锰酸钾溶液氧化生成C,C为CH3COOH,C和乙醇发生酯化反应生成D为CH3COOCH2CH3,据此分析解答.
;B被酸性高锰酸钾溶液氧化生成C,C为CH3COOH,C和乙醇发生酯化反应生成D为CH3COOCH2CH3,据此分析解答.
解答 解:A既是一种重要的化工原料,也是一种水果催熟剂,则A为CH2=CH2,A和水反应生成B,B为CH3CH2OH,A发生加聚反应生成E,E为 ,B在光照条件下发生取代反应生成F,F为CH2ClCH2OH,F在浓硫酸作催化剂加热条件下发生消去反应生成G,G为CH2=CHCl,G发生加聚反应生成H,H为
,B在光照条件下发生取代反应生成F,F为CH2ClCH2OH,F在浓硫酸作催化剂加热条件下发生消去反应生成G,G为CH2=CHCl,G发生加聚反应生成H,H为 ;B被酸性高锰酸钾溶液氧化生成C,C为CH3COOH,C和乙醇发生酯化反应生成D为CH3COOCH2CH3,
;B被酸性高锰酸钾溶液氧化生成C,C为CH3COOH,C和乙醇发生酯化反应生成D为CH3COOCH2CH3,
(1)A是乙烯,含有碳碳双键,
故答案为:碳碳双键;
(2)反应A→E的化学方程式为nCH2=CH2$→_{△}^{催化剂}$ ,
,
故答案为:nCH2=CH2$→_{△}^{催化剂}$ ;
;
(4)乙醇发生催化氧化反应生成乙醛,乙醛被氧化生成乙酸,所以①的反应为2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O;
(5)D为CH3COOCH2CH3,D的能与碳酸氢钠反应即有羧基的同分异构体有CH3CH2CH2COOH、(CH3)2CHCOOH,共两种,
故答案为:2.
点评 本题考查有机物推断,为高频考点,以A为突破口结合反应条件进行推断,熟悉常见有机物结构简式、官能团及其性质关系,题目难度不大.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ | |
| C. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ | |
| D. | 钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解水产生氢气 | |
| B. | 开发特殊物质作催化剂,降低水分解过程中所需要的能量 | |
| C. | 大量建设水电站,用电力分解水制取氢气 | |
| D. | 寻找更多化石燃料,利用燃烧放热,使水分解产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤⑥ | B. | ②③⑤⑥ | C. | ②④⑤⑥ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入少量Na2CO3固体 | B. | 加入少量CuSO4溶液 | ||
| C. | 加入少量NaOH固体 | D. | 加水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大量燃烧化石燃料是造成雾霾天气的原因之一 | |
| B. | 从海水中提取氯化钠、溴、碘不一定都要通过化学反应才能实现 | |
| C. | 燃料脱硫和减少汽车尾气排放都能减少酸雨的产生 | |
| D. | 用高纯度的硅来制备光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由溴乙烷制乙醇;由乙烯与水反应制乙醇 | |
| B. | 乙烯使溴的四氯化碳褪色,甲苯使KMnO4酸性溶液褪色 | |
| C. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯; 苯与液溴在催化剂存下制取溴苯 | |
| D. | 1-氯丙烷与NaOH的乙醇溶液加热反应;l-氯丙烷与NaOH的水溶液加热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com