
 。H2应从电解池的________ (填电极名称)通入;其中b电极的电极反应方程式为________。
。H2应从电解池的________ (填电极名称)通入;其中b电极的电极反应方程式为________。
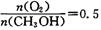 时,制备反应分两步进行,其中一步是
时,制备反应分两步进行,其中一步是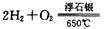
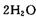 ,则另一步是____________ (写化学方程式)。
,则另一步是____________ (写化学方程式)。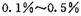 的HCHO可用于杀菌消毒,其原因是________。
的HCHO可用于杀菌消毒,其原因是________。 HCHO+H2 甲醛能使蛋白质变性
HCHO+H2 甲醛能使蛋白质变性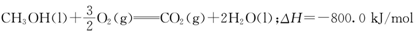 碳粒
碳粒 HCHO+H2。因为甲醛可以使蛋白质变性,所以可用于杀菌消毒。
HCHO+H2。因为甲醛可以使蛋白质变性,所以可用于杀菌消毒。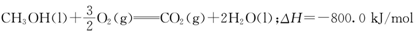 。若氧气不足即相当于燃烧不充分,容易使甲醇被氧化生成碳,从而产生堵塞现象。
。若氧气不足即相当于燃烧不充分,容易使甲醇被氧化生成碳,从而产生堵塞现象。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
 H2+I2
H2+I2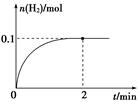
 2HI(g)的平衡常数K= 。
2HI(g)的平衡常数K= 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

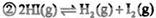
| A.9 | B.16 | C.20 | D.25 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 ?mZ(g) ΔH=-a kJ·mol-1(a>0),现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ;向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是( )
?mZ(g) ΔH=-a kJ·mol-1(a>0),现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2 mol X和1 mol Y,达到平衡状态时,放出热量b kJ;向密闭容器乙中通入1 mol X和0.5 mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是( )| A.m=4 | B.a=b | C.a< | D.m≤2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g)+H2O(g) 。
CH3OH(g)+H2O(g) 。
 CH3OH (g) ΔH=-90.8 kJ·mol-1
CH3OH (g) ΔH=-90.8 kJ·mol-1 CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1 CO2 (g)+H2(g) ΔH=-41.3 kJ·mol-1
CO2 (g)+H2(g) ΔH=-41.3 kJ·mol-1| A.高温高压 |
| B.加入催化剂 |
| C.减少CO2的浓度 |
| D.增加CO的浓度E.分离出二甲醚 |
 CH3OCH3(g)+H2O(g)在某温度下的平衡常数K = 400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)在某温度下的平衡常数K = 400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:| 物质 | CH3OH | CH3OCH3 | H2O |
| c / mol·L-1 | 0.44 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.KW随溶液温度、浓度的改变而改变 |
| B.凡是氧化还原反应,都是放热反应 |
| C.对已达到化学平衡的反应,改变压强,平衡一定改变 |
| D.弱电解质的电离程度,与温度、浓度均有关系 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.增大压强,活化分子百分数不变,化学反应速率增大 |
| B.升高温度,活化分子百分数增大,化学反应速率增大 |
| C.加入反应物,活化分子百分数增大,化学反应速率增大 |
| D.使用催化剂,活化分子百分数增大,化学反应速率增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 ,经过5 min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2 mol /L,求:
,经过5 min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2 mol /L,求:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com