
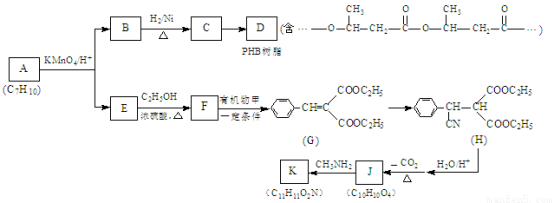
£Ø17·Ö£©PHBŹ÷Ö¬æÉÓĆÓŚÖĘ×÷ĶāæĘŹÖŹõ·ģŗĻĻߣ¬ÓŠ»śĪļKŹĒŅ»ÖÖæ¹¾ŖŲŹŅ©Īļ£¬ĖüĆĒµÄŗĻ³ÉĀ·ĻßČēĻĀ£ŗ
ŅŃÖŖ£ŗ
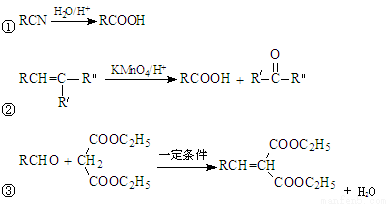
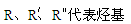
£Ø1£©B”śCµÄ·“Ó¦ĄąŠĶŹĒ ”£
£Ø2£©Š“³öŅ»¶ØĢõ¼žĻĀC”śDµÄ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø3£©ÓŠ»śĪļ¼×µÄ½į¹¹¼ņŹ½ĪŖ ”£
£Ø4£©Š“³öE”śFµÄ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø5£©AµÄ½į¹¹¼ņŹ½ĪŖ ”£
£Ø6£©ŅŃÖŖ1 mol J×ī¶ąÓė2 mol NaHCO3·“Ó¦£»K·Ö×Ó½į¹¹ÖŠŗ¬ÓŠŅ»øöĪåŌŖ»·ÓėŅ»øöĮłŌŖ»·”£Š“³öŅ»¶ØĢõ¼žĻĀJ”śKµÄ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø7£©SŹĒAµÄŅ»ÖÖĶ¬·ÖŅģ¹¹Ģ壬·Ö×Ó֊ƻӊ»·×“½į¹¹£¬SµÄŗĖ“Ź²ÕńĒāĘ×ÓŠČżøö·å£¬·åĆ껿֮±ČĪŖ6:3:1£¬ŌņSµÄ½į¹¹¼ņŹ½ĪŖ £ØŠ“³öŅ»ÖÖ¼“æÉ£©”£
 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ø£½ØŹ”ĖĵŲĮłŠ£ø߶žĻĀѧʌµŚŅ»“ĪĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ·Ö×ÓÖŠµÄÖŠŠÄŌ×ÓµÄŌӻƷ½Ź½ĪŖspŌӻƣ¬·Ö×ÓµÄæռ乹ŠĶĪŖÖ±ĻߊĪĒŅ·Ö×Ó֊ƻӊŠĪ³É¦Š¼üµÄŹĒ
A£®C2H2 B£®BeCl2 C£®CO2 D£®HClO
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ŌĘÄĻŹ”øßŅ»3ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹµŃé²Ł×÷ĖłÓĆŅĒĘ÷ŗĻĄķµÄŹĒ
A£®½«CCl4ÓėäåĖ®»ģŗĻŗóÕńµ“”¢¾²ÖĆ£¬ŌŁÓĆ·ÖŅŗĀ©¶··ÖĄėµĆµ½äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ
B£®ÓĆ100mLČŻĮæĘæÅäÖĘ50mL0.1mol/LNaOHČÜŅŗ
C£®ÓĆĶŠÅĢĢģĘ½³ĘČ”25.30gNaCl
D£®ÓĆ50mLĮæĶ²ĮæČ”4.8mLĮņĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ÉĀĪ÷Ź”±¦¼¦ŹŠøßŅ»4ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖŌ×ÓŠņŹżĪŖaµÄ¢ņA×åŌŖĖŲXŗĶŌ×ÓŠņŹżĪŖbµÄ¢óA×åŌŖĖŲYĪ»ÓŚŌŖĖŲÖÜĘŚ±ķÖŠĶ¬Ņ»ÖÜĘŚ£¬ĻĀĮŠµÄĮæÖµ¹ŲĻµ²»ÕżČ·µÄŹĒ
A£®a£½b£1 B£®a£½b£11
C£®b£½a£«25 D£®b£½a£«30
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ÉĀĪ÷Ź”±¦¼¦ŹŠøßŅ»4ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀ±ķ·ūŗÅÖŠ”°2”±µÄŗ¬ŅåÕżČ·µÄŅ»×éŹĒ
| 2He | Cl2 | Ca2£« | |
A | ÖŹĮæŹż | ÖŠ×ÓŹż | ÖŹ×ÓŹż | µēŗÉŹż |
B | ÖŹĮæŹż | ÖŹ×ÓŹż | Ō×ÓŹż | µēŗÉŹż |
C | ÖŹ×ÓŹż | ÖŠ×ÓŹż | Ō×ÓŹż | µē×ÓŹż |
D | ÖŹĮæŹż | ÖŹ×ÓŹż | ·Ö×ÓŹż | µēŗÉŹż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ±±¾©ŹŠŗ£µķĒųøßČżŅ»Ä£Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®µķ·ŪŗĶĻĖĪ¬ĖŲĖ®½āµÄ×īÖÕ²śĪļ¶¼ŹĒĘĻĢŃĢĒ
B£®æÉŅŌÓĆNaOHČÜŅŗ³żČ„ŅŅĖįŅŅõ„ÖŠµÄŅŅ“¼
C£®ĢģČ»ÓĶÖ¬µÄÖ÷ŅŖ³É·ÖŹĒøß¼¶Ö¬·¾Ėį
D£®CH”ŌCHŗĶCH2=CHCH=CH2»„ĪŖĶ¬ĻµĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ¹ć¶«Õæ½øßČżµŚ¶ž“ĪÄ£Äāæ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¼øÖÖ¶ĢÖÜĘŚŌŖĖŲµÄŌ×Ó°ė¾¶¼°Ö÷ŅŖ»ÆŗĻ¼ŪČēĻĀ±ķ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
ŌŖĖŲ“śŗÅ | X | Y | Z | M | R | Q | |
Ō×Ó°ė¾¶(”Į10£10 m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
Ö÷ŅŖ»ÆŗĻ¼Ū | ×īøßÕż¼Ū | £«1 | £«7 | £«3 | £«2 | £«5 | ”Ŗ”Ŗ |
×īµĶøŗ¼Ū | ”Ŗ”Ŗ | £1 | ”Ŗ”Ŗ | ”Ŗ”Ŗ | -3 | -2 | |
A£®ŌŖĖŲXŗĶQŠĪ³ÉµÄ»ÆŗĻĪļÖŠÖ»ŗ¬ÓŠĄė×Ó¼ü
B£®X”¢Z”¢RµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļÖ®¼äæÉĮ½Į½Ļą»„·“Ó¦
C£®ÓƵ„ÖŹZ×öµÄČŻĘ÷²»ÄÜŹ¢×°ÅØĮņĖį
D£®YµÄĘųĢ¬Ēā»ÆĪļÓėRµÄĘųĢ¬Ēā»ÆĪļÄÜ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğøŹĖąŹ”ĢģĖ®ŹŠøßČżĻĀѧʌ¶žÄ£æ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĪļÖŹÖŠŌÓÖŹ(ĄØŗÅÄŚĪŖŌÓÖŹ)µÄ¼ģŃ锢³żŌӵďŌ¼Į»ņ·½·Ø¶¼ÕżČ·µÄŹĒ
ĪļÖŹ¼°ĘäŌÓÖŹ | ¼ģŃé | ³żŌÓ | |
A | Cl2(HCl) | ŹŖČóµÄµķ·ŪKIŹŌÖ½ | ±„ŗĶŹ³ŃĪĖ® |
B | NO(NO2) | ¹Ū²ģŃÕÉ«»ņŹŖČóµÄµķ·ŪKIŹŌÖ½ | Ė® |
C | CO2(HCl) | AgNO3ČÜŅŗ(ŗ¬Ļ”ĻõĖį) | ±„ŗĶNa2CO3ČÜŅŗ |
D | NaHCO3ČÜŅŗ(Na2CO3) | Ca(OH)2ČÜŅŗ | ¹żĮæCO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ±±¾©ŹŠ·įĢØĒųøßČżµŚ¶ž“ĪÄ£ÄāĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¹¤ŅµÉĻ³£ÓĆ»¹Ō³Įµķ·Ø“¦Ąķŗ¬øõ·ĻĖ®£ØCr2O72”ŖŗĶCrO42”Ŗ£©£¬ĘäĮ÷³ĢĪŖ£ŗ
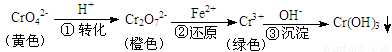
ŅŃÖŖ£ŗ²½Öč¢ŪÉś³ÉµÄCr(OH)3ŌŚČÜŅŗÖŠ“ęŌŚŅŌĻĀ³ĮµķČܽāĘ½ŗā£ŗ
Cr(OH)3(s) Cr3+(aq)+3OH”Ŗ(aq) Ksp=c(Cr3+)”¤c3(OH”Ŗ)=10-32
Cr3+(aq)+3OH”Ŗ(aq) Ksp=c(Cr3+)”¤c3(OH”Ŗ)=10-32
ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ
A£®²½Öč¢ŁÖŠµ±vÕż(CrO42”Ŗ) = 2vÄę(Cr2O72”Ŗ)Ź±£¬ĖµĆ÷·“Ó¦£ŗ2CrO42”Ŗ+2H+ Cr2O72”Ŗ+H2O “ļµ½Ę½ŗāדĢ¬
Cr2O72”Ŗ+H2O “ļµ½Ę½ŗāדĢ¬
B£®ČōĻņK2Cr2O7ČÜŅŗÖŠ¼ÓNaOHÅØČÜŅŗ£¬ČÜŅŗæÉÓɳČÉ«±ä»ĘÉ«
C£®²½Öč¢ŚÖŠ£¬ČōŅŖ»¹Ō1 mol Cr2O72”ŖĄė×Ó£¬ŠčŅŖ12 mol (NH4)2Fe(SO4)2
D£®²½Öč¢ŪÖŠ£¬µ±½«ČÜŅŗµÄpH µ÷½ŚÖĮ5 Ź±£¬æÉČĻĪŖ·ĻĖ®ÖŠµÄøõŌŖĖŲŅŃ»ł±¾³ż¾”£Øµ±ČÜŅŗÖŠc(Cr3+) ”Ü10-5 mol/LŹ±£¬æÉŹÓ×÷øĆĄė×Ó³ĮµķĶźČ«£©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com