
【题目】下列叙述中,正确的是
A. 在船舶的外壳装上铜块可防止其发生电化学腐蚀
B. MnO2、FeCl3和CuSO4都可加快H2O2的分解速率
C. FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3
D. 用惰性电极分别电解CuCl2溶液和MgCl2溶液分别得到单质Cu和Mg
科目:高中化学 来源: 题型:
【题目】某化学小组在实验室中对以SO2的性质进行探究和物质制取.回答下列问题:
(1)① 学生甲以Na2SO3粉未和70% H2SO4为原料制取SO2,下图装置A中仪器X的名称是____;用较浓的硫酸而不用稀硫酸,其原因是________________。
② 现欲收集一瓶干燥的SO2,选择图16,中的装置,其连接顺序为________(按气流方向,用小写字母表示)。

(2)学生乙用浓H2SO4和乙醇反应得到的乙烯气体中含有SO2、CO2。现选择下图中的装置,检验混合气体中存在乙烯和SO2,则装置中盛放的试剂是A______,B______,C______,D______。

(3)Cu2SO3·CuSO3·2H2O是一种深红色固体,不溶于水和乙醇,100℃时发生分解,其制备实验装置如图 所示。
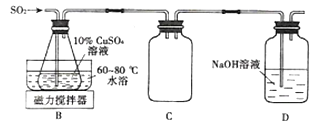
①装置C的作用是______________。
②装置B中发生反应的离子方程式为_______________。
③从装置B中获得的固体需先用蒸馏水充分洗涤,再真空干燥,而不直接用烘干的方式得到产品,其原因是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题: 
(1)该浓盐酸中HCl的物质的量浓度为molL﹣1 .
(2)某学生欲用上述浓盐酸和蒸馏水配制500mL 物质的量浓度为0.400molL﹣1的稀盐酸.
①该学生需要量取mL 上述浓盐酸进行配制.
②在配制过程中,下列实验操作对配制的稀盐酸的物质的量浓度偏小的是
A.用量筒量取浓盐酸进俯视观察凹液面
B.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
C.若容量瓶中洗净后未干燥,残留少量水,则所配制的溶液浓度将
D.定容时,眼睛俯视
E.未冷却到室温就注入容量瓶定容
③配制过程中,所用到的仪器除烧杯、玻璃棒、量筒外还需 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在工农业生产中应用广泛.
(1)根据如图写出合成氨的热化学方程式是____________________.

(2)将1mol N2(g)和3mol H2(g)放在一密闭容器中,进行反应,测得反应放出的热量______(填“大于”、“等于”或“小于”)92.2kJ,原因是______;若加入催化剂,△H__________(填“变大”、“不变”或“变小”).
(3)N2H4可视为NH3分子中的H被﹣NH2取代的产物.发射卫星时以N2H4(g)为燃料、NO2为氧化剂,二者反应生成N2和H2O(g).
已知:N2(g)+2O2(g)═2NO2(g)△H1=+67.7kJmol﹣1
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H2=﹣534kJmol﹣1
则1mol N2H4与NO2完全反应的热化学方程式为______________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com