
| A、含NA个分子的氮气 |
| B、标准状况下3.36L甲烷 |
| C、5.4 g水(水的摩尔质量为18g?mol-1) |
| D、0.4mol三氧化硫 |
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
| A、氯化钠和铁的熔化 |
| B、二氧化硅和生石灰的熔化 |
| C、碘和干冰的升华 |
| D、冰和金刚石 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下11.2 L N2和17 g NH3中所含有的N原子数相同 |
| B、9 g H2O和0.5 mol O2中含的原子数相同 |
| C、20℃时,相同体积的N2、O2一定含有相同的分子数 |
| D、在常温常压下20 mL CH4与60 mL O2所含的原子个数比为1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在28 g乙烯、丙烯和聚乙烯树脂的混合物中,含有的碳原子数目为2NA |
| B、标况下,23g乙醇分子中含有共用电子对数为4NA |
| C、由两种短周期元素X和Y可组成化合物XaYb,当X的原子序数为m时,Y的原子序数可能为:m+8-a-b;m+16-a-b;m-a-b |
| D、同主族元素原子序数差可能为8、18、26、37 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)3胶体粒子所作的布朗运动 |
| B、在电场作用下,Fe(OH)3胶体粒子在分散剂里作定向移动 |
| C、当光束通过Fe(OH)3胶体时,可以看到一条光亮的“通路” |
| D、向Fe(OH)3胶体中逐滴加入盐酸时会观察到先变浑浊再变澄清 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mL 0.1mol?L-1的氯化铝溶液 |
| B、10mL 0.1mol?L-1的氯化钙溶液 |
| C、30mL 0.2mol?L-1的氯化钾溶液 |
| D、40mL 0.25mol?L-1的氯化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、侯氏制碱法的工艺过程中应用了物质溶解度的差异 |
| B、硅胶可以除去氯气中的水蒸气 |
| C、明矾净水属于物理变化 |
| D、黑火药由硫黄、硝石、木炭三种物质按一定比例混合制成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若m+n<p,温度不变,将容器体积缩小到原来的一半,则X的浓度大于原来的2倍 |
| B、若在密闭恒温容器中加入pmol的Z达到平衡,再加入一定量的Z,Z的百分比含量不变,则m+n=p |
C、若定温下Y的体积分数(Y%)与压强变化的关系如图所示,则a点表示平衡正向移动且反应速率:a点<b点 |
| D、若m+n=p,且在密闭恒容容器内进行,当温度升高时,平衡逆向移动,容器中气体的压强不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
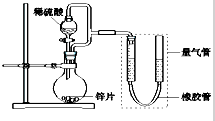 某同学设计如图所示装置(部分夹持装置已略去),该装置可以用来进行多项实验研究.
某同学设计如图所示装置(部分夹持装置已略去),该装置可以用来进行多项实验研究.| 序号 | V(H2SO4)/ml | C(H2SO4)/mol?L-1 | t/s |
| Ⅰ | 40 | 1 | t1 |
| Ⅱ | 40 | 4 | t2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com