
【题目】今年6月20日,2016年全球最受关注的十大化学成果发布,其中有两项与空气中的二氧化碳处理利用技术有关。其一为美国伊利诺斯大学芝加哥分校和阿贡国家实验室科学家联合设计的新型太阳能电池,可直接把大气中的二氧化碳转化为合成气(CO和H2)该设计同时具有环保和经济价值,不仅可以减缓二氧化碳的排放,而且可以生成重要的化工原料。
(1)下列材料也可以用于制造太阳能电池的是____________。
A.Ag2O B.Fe3O4 C.Si D.SiO2
(2)下图装置可实现二氧化碳到一氧化碳的转化
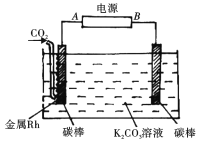
①电源的正极为______(“A”或“B")。
②阴极发生反应的电极方程式为:___________.
(3)CO 和H2可用于合成甲醇。
①已知CO、H2、CH3OH(1)的燃烧热为283.0kJ/mol、285.8kJ/mol、726.5kJ/mol,写出 由CO和H2制备CH3OH(1)的热化学方程式__________。
②在398K,1L的恒容容器中充入0.1molCO和0.2molH2,发生反应CO(g)+2H2(g) ![]() CH3OH(g),反应过程中气体的压强如下表所示(atm为标准大气压)。
CH3OH(g),反应过程中气体的压强如下表所示(atm为标准大气压)。
时间(min) | 0 | 1 | 5 | 10 | 30 | 50 |
压强(atm) | 10 | 9.3 | 8.0 | 7.2 | 4 | 4 |
该温度下的平衡常数是_____。达到平衡后,向该容器中通入0.05mol的气态CH3OH,再次达到平衡时,CH3OH的体积分数比原平衡时_____( 填“大”或“小”)。
【答案】C B CO2+ H2O+2e-=CO+2OH- CO(g)+2H2(g)=CH3OH(l) △H=-128.1kJ·mol-1 2.25×104 大
【解析】
(1)所列材料中硅是非常重要的半导体材料,可以用于制造太阳能电池,选C。
(2)由图中信息可知,该装置为电解池,与A相连的电极上发生二氧化碳到一氧化碳的转化,二氧化碳被还原,所以该电极是电解池的阴极, A为电源负极。①电源的正极为B。②因为电解质溶液是呈碱性的碳酸钾溶液,所以阴极发生反应的电极方程式为: CO2+ H2O+2e-=CO+2OH-.
(3)①已知CO、H2、CH3OH(1)的燃烧热为283.0kJ/mol、285.8kJ/mol、726.5kJ/mol,则有(a)CO(g)+1/2O2(g)=CO2(g) △H=-283.0kJ/mol、(b)H2(g)+1/2O2(g)=H2O(l) △H=-285.8kJ/mol、(c)CH3OH(1)+3/2O2(g)=CO2(g)+2H2O(l) △H=-726.5kJ/mol,由a+2b-c得,CO(g)+2H2(g)=CH3OH(l) ,所以△H=(-283.0kJ/mol)+2![]() (-285.8kJ/mol)-(-726.5kJ/mol)-128.1kJ·mol-1。所以由CO和H2制备CH3OH(1)的热化学方程式为CO(g)+2H2(g)=CH3OH(l) △H=-128.1kJ·mol-1。
(-285.8kJ/mol)-(-726.5kJ/mol)-128.1kJ·mol-1。所以由CO和H2制备CH3OH(1)的热化学方程式为CO(g)+2H2(g)=CH3OH(l) △H=-128.1kJ·mol-1。
②在398K,1L的恒容容器中充入0.1molCO和0.2molH2,发生反应CO(g)+2H2(g) ![]() CH3OH(g), 由表中数据可知,该反应在30min时达到平衡,平衡时的压强是反应前的40%,所以反应混合物的总物质的量也是反应前的40%.设反应中CO的变化量为x,则H2和CH3OH的变化量分别为2x和x,则(0.1mol-x)+(0.2mol-2x)+x=(0.1mol+0.2mol)
CH3OH(g), 由表中数据可知,该反应在30min时达到平衡,平衡时的压强是反应前的40%,所以反应混合物的总物质的量也是反应前的40%.设反应中CO的变化量为x,则H2和CH3OH的变化量分别为2x和x,则(0.1mol-x)+(0.2mol-2x)+x=(0.1mol+0.2mol)![]() ,解之得,x=0.09mol,则CO、H2、CH3OH的平衡浓度分别为0.01 mol/L、0.02 mol/L、0.09mol/L,所以该温度下的平衡常数K=
,解之得,x=0.09mol,则CO、H2、CH3OH的平衡浓度分别为0.01 mol/L、0.02 mol/L、0.09mol/L,所以该温度下的平衡常数K=![]() 2.25×104。达到平衡后,向该容器中通入0.05mol的气态CH3OH,再次达到平衡时,根据平衡移动原理可以判断,CH3OH的体积分数比原平衡时大。
2.25×104。达到平衡后,向该容器中通入0.05mol的气态CH3OH,再次达到平衡时,根据平衡移动原理可以判断,CH3OH的体积分数比原平衡时大。


科目:高中化学 来源: 题型:
【题目】常温下将体积都为10mL、pH都等于3的醋酸和盐酸,加水稀释至a mL和b mL,测得稀释后溶液的pH均为5,则稀释后溶液的体积为 ( )
A.a>bB.a<bC.a<b<100mLD.a=b=100mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A与D是常见的有机化工原料,下列路线合成香料M(![]() ):
):

已知以下信息:
①A的相对分子质量为28
②2RCH2CHO![]()

(1)A的结构简式是________,D的名称是__________。
(2)A生成B的反应类型为_____________,G中官能团名称为___________。
(3)E生成F的的化学方程式为_________________________________________。
(4)下列关于G的说法正确的是______________。(填标号)
a.属于芳香烃
b.可与FeCl3溶液反应显紫色
c.1molG与H2完全加成,最多4molH2
d.可与新制的氢氧化铜共热生成红色沉淀
(5)化合物M的同系物N比M的相对分子质量大14,N的同分异构体中同时满足下列条件的共有__________种(不考虑立体构)。
①与化合物M含有相同的官能团; ②苯环上有两个邻位取代基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X+的核外电子数分别为2、8、8,则X元素在周期表中的位置是( )
A. 第三周期第0族 B. 第四周期第ⅠA族
C. 第三周期第ⅠA族 D. 第三周期第ⅦA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表。下列判断不正确的是
A. a=6.00 B. 同时改变反应温度和蔗糖的浓度,v可能不变
C. b<50 D. 50℃时,经过5s蔗糖浓度减少一半
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下、一定体积条件下,能说明下列反应达到平衡状态的是
A.反应2SO2(g)+O2(g)![]() 2SO3(g) 容器内的密度不随时间变化
2SO3(g) 容器内的密度不随时间变化
B.反应A2(g)+B2(g)![]() 2AB(g)容器内A2的消耗速率与AB消耗速率相等
2AB(g)容器内A2的消耗速率与AB消耗速率相等
C.反应N2+3H2![]() 2NH3容器内气体平均相对分子质量不随时间变化
2NH3容器内气体平均相对分子质量不随时间变化
D.反应4A(s)+3B(g)![]() 2C(g)+D(g)容器内气体总压强不随时间变化
2C(g)+D(g)容器内气体总压强不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸,又称草酸,通常在空气中易被氧化而变质。其两分子结晶水(H2C2O4·2H2O)却能在空气中稳定存在。在分析化学中常用H2C2O4·2H2O做KMnO4的滴定剂,下列关于H2C2O4的说法正确的是
A.草酸是二元弱酸,其电离方程式为H2C2O4![]() 2H++C2O
2H++C2O![]()
B.草酸滴定KMnO4属于中和滴定,可用石蕊做指示剂
C.乙二酸可通过乙烯经过加成、水解、氧化再氧化制得
D.将浓H2SO4滴加到乙二酸上使之脱水分解,分解产物是CO2和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是甲烷(CH4)和白磷(P4)分子的空间结构示意图,请把你认为是化学键的虚线改为实线,把碳原子涂成实心小圆点(在图上改即可__________)。甲烷分子是________(填“左”、“右”)图。从图中看出,每个甲烷分子中有________对共用电子,而白磷分子中形成______个共价键,键角为________。甲烷是由________键(填“极性”或“非极性”,下同)形成的________分子,白磷是由________键形成的________分子。
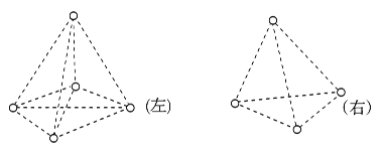
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年7月报道,南开大学科研团队在“可充室温钠-二氧化碳电池”的研究中取得突破进展,该电池放电时工作情况如图所示。下列说法错误的是

A. 金属Na为电池的负极
B. 放电时,电解液中Na+向碳电极移动
C. 充电时,碳电极发生的反应为:4Na++4e-+3CO2== 2Na2CO3+C
D. 放电时,每转移2 mol电子,消耗标准状况下的CO2 33.6 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com