
请用核外电子排布的相关规则解释Fe3+较Fe2+更稳定的原因。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
写出下列典型物质的电离方程式
(1)H2SO4______________________________________________________________________;
(2)H2CO3______________________________________________________________________;
(3)Ca(OH)2____________________________________________________________________;
(4)Fe(OH)3_____________________________________________________________________;
(5)NH3·H2O____________________________________________________________________;
(6)NaCl_______________________________________________________________________;
(7)BaSO4_____________________________________________________________________;
(8)NaHSO4_____________________________________________________________________;
(9)NaHCO3____________________________________________________________________;
(10)NaHSO4(熔融)_____________________________________________________________;
(11)Al2O3(熔融)___________________________________________________________;
(12)CH3COOH_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于晶体的说法,一定正确的是 ( )。
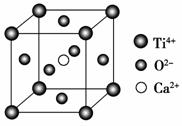
CaTiO3的晶体结构模型(图中Ca2+、O2-、
Ti4+分别位于立方体的体心、面心和顶角)
A.分子晶体中都存在共价键
B.如上图,CaTiO3晶体中每个Ti4+和12个O2-相紧邻
C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合
D.金属晶体的熔点都比分子晶体的熔点高
查看答案和解析>>
科目:高中化学 来源: 题型:
元素的原子半径在周期表中呈现周期性变化的根本原因是( )
A.原子的相对原子质量呈现周期性变化
B.元素的化合价呈现周期性变化
C.原子的性质呈现周期性变化
D.元素原子的核外电子排布呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻。X的核电荷数是Y的核外电子数的一半,Y与M可形成化合物M2Y。下列说法正确的是( )
A.还原性:X的氢化物>Y的氢化物>Z的氢化物
B.简单离子的半径:M的离子>Z的离子>Y的离子>X的离子
C.YX2、M2Y都是含有极性键的极性分子
D.Z元素的最高价氧化物的水化物的化学式为HZO4
查看答案和解析>>
科目:高中化学 来源: 题型:
根据前四周期元素原子核外电子排布特点,回答下列问题:
(1)外围电子层有2个未成对电子的有________;有3个未成对电子的有________。
(2)未成对电子数与周期数相等的元素有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,不符合ⅦA族元素性质特征的是( )
A.从上到下原子半径逐渐减小
B.易形成-1价离子
C.从上到下单质的氧化性逐渐减弱
D.从上到下氢化物的稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
试比较下列各组ΔH的大小。
(1)同一反应,生成物状态不同时
A(g)+B(g)===C(g) ΔH1<0
A(g)+B(g)===C(l) ΔH2<0
则ΔH1____ΔH2(填“>”、“<”或“=”,下同)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com