
【题目】一定温度下,在三个容积均为2L的恒容密闭容器中按不同方式投入反应物,发生反应:2CO(g) + 4H2(g)CH3OCH3(g) + H2O(g) △H<0,测得反应的相关数据如下表:
容器1 | 容器2 | 容器3 | |
反应温度T/K | 600 | 600 | 500 |
反应物投入量 | 0.2mol CO 0.4mol H2 | 0.4mol CO 0.8mol H2 | 0.2mol CH3OCH3 0.2mol H2O |
平衡v(CO)/(mol·L-1·s-1) | v1 | v2 | v3 |
平衡n(H2)/(mol) | 0.2 | n2 | n3 |
平衡体系总压强p/Pa | p1 | p2 | p3 |
物质的平衡转化率a | a1(CO) | a2(CO) | a3(CH3OCH3) |
平衡常数K | K1 | K2 | K3 |
下列说法正确的是
A.v1<v2,n2>0.4B.K2=2.5×103,p2>p3
C.2p1<p3,a1(CO) >a2(CO)D.n3<0.4,a2(CO) + a3(CH3OCH3)<1
【答案】BD
【解析】
A.容器1和容器2温度相同,但容器2内浓度更大,反应速率更快,所以v1<v2;若容器2的容积为容器1的二倍,则二者达到等效平衡,n2=0.4,但实际上容器2容积与容器1相等,相当于在等效平衡的基础上进行加压,该反应为气体系数减小的反应,加压平衡正向移动,则n2<0.4,故A错误;
B.温度相同平衡常数相同,所以K1=K2,对于容器1,投料为0.2mol CO,0.4mol H2,平衡时n(H2)=0.2mol,容器体积为2L,列三段式有

所以平衡常数K1=![]() =2.5×103,即K2=2.5×103;
=2.5×103,即K2=2.5×103;
将容器3的投料极限转化后和容器2投料相同,若二者反应温度相同,则达到等效平衡,此时p2=p3,但实际上容器3温度降低,该反应正反应为放热反应,降低温度平衡正向移动,导致压强减小,所以p2>p3,故B正确;
C.若容器3与容器1反应温度相同,且容积为容器1的2倍,则二者达到等效平衡,此时p1=p3,但实际上二者容积相等,假设把容积压缩到与1相等的过程中平衡不移动,此时2p1=p3,但实际加压平衡会正向移动,所以2p1>p3,且温度降低平衡正向移动,导致p3进一步减小;
根据A选项分析可知a1(CO) <a2(CO),故C错误;
D.根据C选项分析,容器3相当于容器1的等效平衡状态正向移动,所以n3<0.4;容器2和3若为等效平衡,则a2(CO)+a3(CH3OCH3)=1,根据B选项分析可知容器3相当于容器2的等效平衡状态正向移动,a3(CH3OCH3)减小,所以a2(CO)+a3(CH3OCH3)<1,故D正确;
故答案为BD。


科目:高中化学 来源: 题型:
【题目】如图所示,隔板I固定不动,活塞II可自由移动,M、N两个容器中均发生反应:A(g)+2B(g)![]() xC(g),向M、N中通入1mol和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是( )
xC(g),向M、N中通入1mol和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是( )

A. 若x=3,达到平衡后A的体积分数关系为:![]()
B. 若x<3,C的平衡浓度关系为:c(M)<c(N)
C. 若x>3,达到平衡后B的转化率关系为:![]()
D. x不论为何值,平衡时M、N中的平均相对分子质量都相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种电化学“大气固碳”电池工作原理如图所示。该电池在充电时,通过催化剂的选择性控制,只有Li2CO3发生氧化,释放出CO2和O2。下列说法正确的是
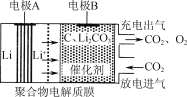
A.该电池放电时的正极反应为2Li-2e-+CO32-=Li2CO3
B.该电池既可选用含水电解液,也可选无水电解液
C.充电时阳极发生的反应为C+2Li2CO3-4e-=3CO2+4Li+
D.该电池每放、充4 mol电子一次,理论上能固定1 mol CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图,判断下列叙述中正确的是
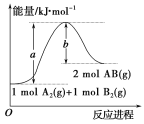
A.该反应的活化能是b kJ/mol
B.该反应热ΔH=+(a-b)kJ/mol
C.该反应中反应物的总能量高于生成物的总能量
D.1molA2(g)和1molB2(g)的能量总和是akJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向温度为300℃的2L密闭容器中充入2molSO2和1molO2发生反应:![]() ,体系达到平衡状态后SO2的浓度为0.1mol/L,下列说法错误的是
,体系达到平衡状态后SO2的浓度为0.1mol/L,下列说法错误的是
A. 该温度下反应的平衡常数K=1620
B. SO2和O2的平衡转化率相等
C. 平衡后保持温度和容器体积不变再充入SO3(g),平衡逆向移动且平衡常数不变
D. 若不再向容器中加入任何物质,改变条件不可能使SO2的浓度达到1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤会产生![]() 、CO、
、CO、![]() 等大气污染物。燃煤脱硫的相关反应的热化学方程式如下:
等大气污染物。燃煤脱硫的相关反应的热化学方程式如下:
Ⅰ.![]()
Ⅱ.![]()
(1)一定温度下,向某恒容密闭容器中加入![]() 和1molCO,若只发生反应Ⅰ,下列能说明该反应已达到平衡状态的是______
和1molCO,若只发生反应Ⅰ,下列能说明该反应已达到平衡状态的是______![]() 填序号
填序号![]()
![]() 容器内的压强不发生变化
容器内的压强不发生变化
b.![]()
![]() 容器内气体的密度不发生变化
容器内气体的密度不发生变化
d.![]()
(2)一定温度下,体积为1L容器中加入![]() 和1molCO,若只发生反应Ⅱ,测得
和1molCO,若只发生反应Ⅱ,测得![]() 的物质的量随时间变化如图中曲线A所示:
的物质的量随时间变化如图中曲线A所示:
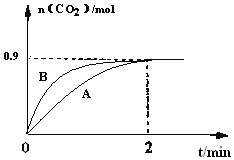
①在![]() 内的平均反应速率
内的平均反应速率![]() ______。
______。
②曲线B表示过程与曲线A相比改变的反应条件可能为______![]() 答出一条即可
答出一条即可![]() 。
。
③若要提高反应体系中![]() 的体积分数,可采取的措施为______。
的体积分数,可采取的措施为______。
(3)一定温度下,向恒容密闭容器中加入![]() 和1molCO,下列能说明反应I和反应II同时发生的是______
和1molCO,下列能说明反应I和反应II同时发生的是______![]() 填代号
填代号![]() 。
。
![]() 反应后气体能使品红褪色
反应后气体能使品红褪色
![]() 反应过程中,CO的体积分数逐渐减小
反应过程中,CO的体积分数逐渐减小
![]() 反应体系达平衡前,
反应体系达平衡前,![]() 和
和![]() 两种气体的浓度之比随时间发生变化
两种气体的浓度之比随时间发生变化
![]() 体系压强逐渐增大
体系压强逐渐增大
(4)烟道气中的![]() 和
和![]() 均是酸性氧化物,也可用氢氧化钠溶液吸收。
均是酸性氧化物,也可用氢氧化钠溶液吸收。
已知:![]() 时,碳酸和亚硫酸的电离平衡常数分别为:
时,碳酸和亚硫酸的电离平衡常数分别为:
碳酸 ![]()
亚硫酸 ![]()
①下列事实中,不能比较碳酸与亚硫酸的酸性强弱的是______![]() 填标号
填标号![]() 。
。
![]() 下,饱和碳酸溶液pH大于饱和亚硫酸溶液pH
下,饱和碳酸溶液pH大于饱和亚硫酸溶液pH
![]() 下,等浓度的
下,等浓度的![]() 溶液pH大于
溶液pH大于![]() 溶液
溶液
![]() 将
将![]() 气体通入
气体通入![]() 溶液,逸出气体通入澄清石灰水,澄清石灰水变浑浊
溶液,逸出气体通入澄清石灰水,澄清石灰水变浑浊
![]() 将
将![]() 气体通入
气体通入![]() 溶液,逸出气体通入品红溶液,品红溶液不褪色
溶液,逸出气体通入品红溶液,品红溶液不褪色
②![]() 时,氢氧化钠溶液吸收烟道气,得到
时,氢氧化钠溶液吸收烟道气,得到![]() 的吸收液,该溶液中
的吸收液,该溶液中![]() :
:![]() ______。
______。
③少量![]() 溶液和
溶液和![]() 溶液反应的离子方程式为______。
溶液反应的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列填空:
(1)与标准状况下4.48LCO2中所含氧原子数目相同的水的质量是__g;
(2)VLFe2(SO4)3溶液中含Fe3+mg,则溶液中SO42-的物质的量浓度为__mol/L;
(3)氧化铜在高温下发生分解反应:4CuO![]() 2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为__。(阿伏伽德罗常数为NA)。
2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为__。(阿伏伽德罗常数为NA)。
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了__性和__性,则56gFe参加反应时,被还原的HNO3为__g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:
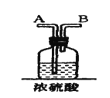
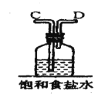
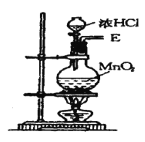
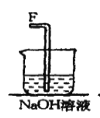
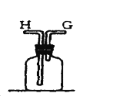
(1)该反应中生成氯气的化学方程式为:__。
(2)连接上述仪器的正确顺序是:(填各接口处的字母)E接___接___,___接___接___,___接__。___。
(3)在装置中,①饱和食盐水起的作用是__。
②浓硫酸起的作用是__。
③NaOH溶液的作用是__。
(4)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温度下,将Cl2缓慢通入水中至饱和,然后再滴加0.1mol/L的NaOH溶液,整个过程中溶液的pH变化曲线如图所示。已知d点所示的溶液中,钠元素与氯元素的物质的量相等,下列选项正确的是( )
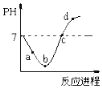
A.a点时,已经滴入NaOH溶液
B.b点所示的溶液中,只存在两种分子
C.a、b、c、d四个点当中,d点水的电离程度最大
D.c点所示的溶液中,c(Na+)=c(Cl-)+c(HClO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com