
下面有关晶体的叙述中,错误的是
A.金刚石网状结构中,碳原子和共价键的个数比为1:2
B.氯化钠晶体中,每个Na+周围紧邻且等距离的Cl-构成的空间结构为立方体
C.氯化铯晶体中,每个Cs+周围紧邻6个Cs+
D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
科目:高中化学 来源: 题型:
某溶液中只可能含有K+、NO3−、SO42−、NH4+、CO32−中的几种(不考虑少量的H+与OH−),取200 mL该溶液分成两等份,进行如下实验:一份加入足量烧碱并加热,产生气体在标准状况下为224 mL;另一份先加足量盐酸无现象,再加入足量BaCl2得到2.33 g固体,则该溶液中
A.可能含有K+ B.肯定含有NO3−、SO42−、NH4+、CO32−
C.一定不含有NO3− D.一定含有K+
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是短周期的元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。下列说法正确的是( )
A.原子半径由小到大的顺序为X<Y<Z<W
B.Z的最高价氧化物能与水反应生成相应的酸
C.X、Z、W最高价氧化物对应水化物酸性的强弱顺序为Z<X<W
D.室温下,0.1 mol/L W的气态氢化物的水溶液的pH>1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关晶体的说法中正确的是
A.氯化钾溶于水时离子键未被破坏 B.原子晶体中共价键越强,熔点越高
C.冰融化时分子中共价键发生断裂 D.范德华力越大,分子越稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
表中原子化热、晶格能、键能的单位都是kJ·mol-1
| 金属 | 金属原子化热 | 离子化合物 | 晶格能 | 共价键 | 键能 |
| Na | 108.4 | NaCl | 786 | Cl-Cl | 243 |
| Mg | 146.4 | NaBr | 747 | Si-Si | 176 |
| Al | 326.4 | MgO | 3791 | Si-Cl | 360 |
则下列说法正确的是
A.Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量为556.1kJ
B.Si(s)+2Cl2(g)=SiCl4(g) △H= - 602kJ·mol-1
C.从表中可以看出,氯化钠的熔点比晶体硅高
D.从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图所示,烧杯中都盛有稀硫酸。
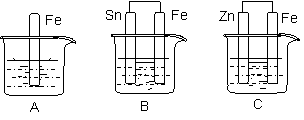 |
(1)A中反应的离子方程式为 ;
(2)B中的电极反应:Fe: 、Sn: 、Sn极附近溶液的pH(填增大、减小或不变) ;
(3)C中被腐蚀的金属是 、其电极反应式为 。
比较A、B、C中纯铁被腐蚀的速率由快到慢的顺序是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com