
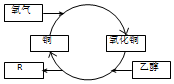
| A. | R的化学式为C2H4O | |
| B. | 乙醇发生了还原反应 | |
| C. | 反应过程中固体有红黑交替变化的现象 | |
| D. | 乙二醇(HO-CH2-CH2-OH)也能发生类似反应 |
分析 依据图中转化过程可知:铜与氧气反应生成氧化铜,氧化铜与乙醇发生反应生成铜与R,结合乙醇的催化氧化反应及氧化还原反应基本概念判断解答.
解答 解:依据图中转化过程可知:铜与氧气反应生成氧化铜,氧化铜与乙醇发生反应生成铜与R,
A.氧化铜与乙醇发生反应生成铜与R,反应中铜元素化合价降低,发生还原反应,则乙醇发生氧化反应,生成乙醛,分子式为:C2H4O,故A正确;
B.氧化铜与乙醇发生反应生成铜和乙醛,氧化铜在反应中发生还原反应,乙醇在反应中发生氧化反应,故B错误;
C.铜为红色,与氧气反应生成黑色的氧化铜,黑色氧化铜与乙醇发生反应,生成铜,所以现象:固体有红黑交替变化,故C正确;
D.乙二醇与乙醇结构相似,也能发生催化氧化生成乙二醛,故D正确;
故选:B.
点评 本题以框图推断为载体考查了乙醇的催化氧化,明确乙醇的结构特点及催化氧化反应原理是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
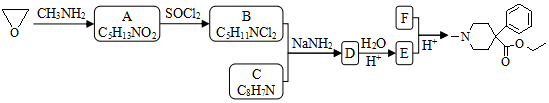
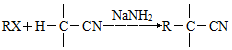
 .
.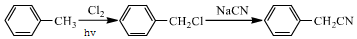 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5 mol | |
| B. | 28g乙烯和环丙烷(C3H6)组成的混合气体,完全燃烧时,转移的电子数为12NA | |
| C. | 0.1 mol•L-1的(NH4)2SO4溶液中,所含NH4+数小于0.2NA | |
| D. | 标准状况下,2.24 L18O2中含有2NA个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅熔点高,可制玻璃仪器 | B. | NaHCO3受热分解,可焙制糕点 | ||
| C. | N2化学性质稳定,可作保护气 | D. | 明矾易水解生成胶体,可作净水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,3.36LC2H4和C3H6的混合气体中含有碳碳双键的数目为0.15NA | |
| B. | 0.1 mol•L-1(NH4)2SO4溶液与0.2 mol•L-1NH4CI溶液中的NH4+数目相同 | |
| C. | H2和CO混合气体8.96 L在足量O2中充分燃烧消耗O2分子数为0.2 NA | |
| D. | 含0.1molNH4HSO4的溶液中,阳离子数目略大于0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
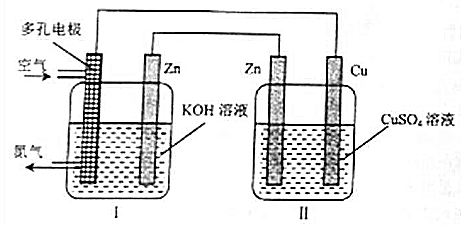
| A. | Cu电极质量增加 | |
| B. | 装置Ⅱ将化学能转变为电能 | |
| C. | 装置Ⅰ中OH-向多孔电极移动 | |
| D. | 多孔电极的电极反应式为:O2+4e-+2H2O═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
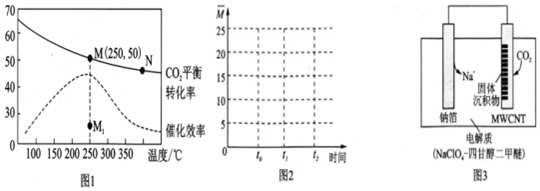
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y、Z、W的简单离子半径Z>W>Y | B. | 工业上制取Y可用电解YW3制得 | ||
| C. | XW2中各原子均达到8电子结构 | D. | Z、W的氧化物对应水化物的酸性Z<W |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com