
| 用Pt丝灼烧 |
| ① |
| +氯化钡溶液 |
| ② |
| +稀HCl酸化 |
| ③ |
| +稀氨水 |
| ④ |
| +烧碱溶液 |
| ⑤ |
| 通入过量CO2 |
| ⑥ |
| A、该无色溶液不可能是明矾溶液 |
| B、这三组实验中,只有(3)是严密合理的 |
| C、步骤④的离子方程式为:Al3++3OH-=Al(OH)3↓ |
| D、步骤⑥的化学方程式为:NaAlO2+H2O+CO2=Al(OH)3↓+NaHCO3 |
| 用Pt丝灼烧 |
| ① |
| +氯化钡溶液 |
| ② |
| +稀HCl酸化 |
| ③ |
| +稀氨水 |
| ④ |
| +烧碱溶液 |
| ⑤ |
| 通入过量CO2 |
| ⑥ |


科目:高中化学 来源: 题型:
| A、开始反应时,二者的速率相等 |
| B、盐酸放出的H2多 |
| C、二者放出的H2一样多 |
| D、醋酸消耗的Zn的质量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素X在周期表中的位置为第2周期VIA族 |
| B、元素X、Y、Z的原子半径由大到小的顺序为r(Z)>r(Y)>r(X) |
| C、1mol甲与足量的乙完全反应转移的电子数为6.02×1023 |
| D、1.0L 0.1mol?L-1戊溶液中阴离子的总物质的量小于0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、固体A主要是SiO2 |
| B、固体X主要是Fe(OH)3和Mg (OH)2 |
| C、滤液D中通入过量CO2发生的主要反应为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3 |
| D、滤液E中含有NaHCO3,NaHCO3是焙制糕点所用的发酵粉的主要成分之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:
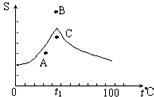 Na2SO4溶液的溶解度曲线如图,下列说法一定错误的是( )
Na2SO4溶液的溶解度曲线如图,下列说法一定错误的是( )| A、A点表示Na2SO4溶液尚未达到饱和,但降温和加入Na2SO4?H2O晶体都可使其饱和 |
| B、B、C点表示t1℃时,Na2SO4溶液在B点的溶解度大于在C点的溶解度 |
| C、在C点时Na2SO4溶液降温或升温,都会使其溶液变浑浊 |
| D、制取芒硝的最佳方法是在100℃时配成饱和溶液,再降温至0℃析出晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 观察图,讨论:
观察图,讨论:查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H2)?c(CO) |
| c(H2O) |
| n(CH4) |
| n(H2O) |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com