
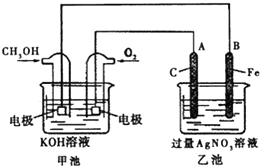
 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中的信息,填写空格.分析 (1)依据铅蓄电池的电池总反应式分析,放电时,Pb在负极失电子发生氧化反应;
(2)①放电时,负极上甲醇失电子发生氧化反应;充电时,原电池正极与电源正极相连;
②氢氧根在阳极上失电子发生氧化反应生成氧气;
③乙池阴极上银离子得电子发生还原反应使电极增重,与源电池的负极相连的电极为阴极,根据转移电子相等计算氧气的体积;
④电解精炼银时,粗银作阳极,精银作阴极.
解答 解:(1)铅蓄电池的电池总反应式为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,依据反应的总电池反应,反应中Pb元素化合价升高的在负极失电子发生氧化反应,其电极反应为:Pb+SO42--2e-=PbSO4,
故答案为:Pb+SO42--2e-=PbSO4;
(2)①放电时,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,所以电极反应式为:CH3OH-6e-+8OH-═CO32-+6H2O,充电时,原电池正极与电源正极相连,
故答案为:CH3OH-6e-+8OH-═CO32-+6H2O;正;
②阳极上氢氧根离子失电子发生氧化反应,电极反应式为:4OH--4e-═2H2O+O2↑,
故答案为:4OH--4e-═2H2O+O2↑;
③在阴极上银离子得电子发生还原反应使电极增重,与源电池的负极相连的电极为阴极,所以是乙池中B极增重,当增重648g时,根据 O2~4e-~4Ag可知甲池中理论上消耗O2体积为 $\frac{648g}{108g/mol}÷4×22.4L/mol$=33.6L,
故答案为:B;33.6;
④用乙池电解精炼银,A是电解池的阳极,所以A为粗银,B是解池的阴极,所以B是精银或纯银,
故答案为:粗银;粗银(或纯银).
点评 本题考查了原电池和电解池原理,注意电极反应式的书写要结合电解质溶液的酸碱性,串联电路中转移电子相等,难度中等.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:选择题
| A. | H2燃烧生成1 mol H2O(g)时,放出241.8 kJ的热量 | |
| B. | O2前面的$\frac{1}{2}$表示参加反应的O2的分子数目 | |
| C. | 燃烧热是以在101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量定义的,则 H2的燃烧热为285.8 kJ•mol-1 | |
| D. | 1 mol H2和$\frac{1}{2}$ mol O2所具有的总能量大于1mol H2O(g)所具有的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,下列叙述中正确的是( )
,下列叙述中正确的是( )| A. | 1mol胡椒酚最多可与5molH2发生反应 | |
| B. | 1mol胡椒酚最多可与4mol溴发生反应 | |
| C. | 胡椒酚中所有原子可以共平面 | |
| D. | 胡椒酚在水中的溶解度小于苯酚在水中的溶解度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①不正确 | B. | ②⑤不正确 | C. | 只有③④正确 | D. | 全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 不纯物 | 除杂试剂 | 分离方法 |
| A | CH4 (C2H4) | 酸性KMnO4溶液 | 洗气 |
| B | NH4Cl溶液 (FeCl3) | NaOH溶液 | 过滤 |
| C | 乙酸乙酯 (乙酸) | 饱和Na2CO3溶液 | 蒸馏 |
| D | C2H5OH (H2O) | 新制生石灰 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量比是9:22 | B. | 相同条件下的密度一定相同 | ||
| C. | 原子个数不同 | D. | 相同条件下体积一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.24mol | B. | 0.21mol | C. | 0.25mol | D. | 0.12mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com