
【题目】某同学对教材中铜与浓硫酸的实验作出如下改进。实验装置如图所示(加热和夹持装置已略去)。
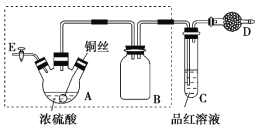
实验步骤:
①组装仪器,检查装置气密性;
②加入试剂,关闭旋塞E,加热A,观察C中溶液颜色变化;
③将铜丝上提离开液面,停止加热。
(1)检查虚线框内装置气密性的方法是____________________________。
(2)装置A的名称是________,装置B的作用是_________,装置D中所盛药品是__________。
(3)装置A中发生反应的化学方程式为____________________________。
(4)实验后,拆除装置前,为避免有害气体的泄漏,应当采取的操作是__________。
(5)实验后装置A中有白色固体产生,将装置A中固液混合物缓慢转移至盛有少量水的烧杯中,可观察到的现象是______________;不可直接向装置A中加水的原因是__________。
【答案】关闭旋塞E,装置C中加水没过导管口,给A装置微热,装置C中导管口有气泡冒出,撤去热源后,导管内有倒吸产生的液柱,且高度保持不变 三颈烧瓶; 防倒吸 碱石灰 Cu+2H2SO4═CuSO4+SO2↑+2H2O 打开旋塞E,从E管口向A中鼓入大量空气 混合时放热,白色固体溶解,溶液变蓝色 水加入浓硫酸中,放出大量热使液体飞溅
【解析】
(1)装置气密性检验的原理是:通过气体发生器与附设的液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏;
(2)仪器A的名称是三颈烧瓶,仪器B的作用是防止二氧化硫倒吸,仪器D是处理尾气,而二氧化硫是酸性气体,所以D中所盛药品是碱石灰或NaOH固体;
(3)铜与浓硫酸在加热的条件下生成硫酸铜、二氧化硫和水;
(4)从E处鼓入空气或氮气,使体系中的二氧化硫完全除净;
(5)硫酸铜晶体溶于水溶液变蓝色;铜元素的焰色反应呈黄绿色,水加入浓硫酸中,放出大量热使液体飞溅.
(1)对于简易装置的气密性检查时,一般对瓶内气体加热,然后看有无气泡冒出或冷却后看导管口是否形成一段水柱,所以要关闭旋塞E,装置C中加水没过导管口,给A装置微热,装置C中导管口有气泡冒出,撤去热源后,导管内有倒吸产生的液柱,且高度保持不变;
故答案为:关闭旋塞E,装置C中加水没过导管口,给A装置微热,装置C中导管口有气泡冒出,撤去热源后,导管内有倒吸产生的液柱,且高度保持不变;
(2)仪器A的名称是三颈烧瓶,仪器B的作用是防止二氧化硫倒吸,仪器D是尾气处理,而二氧化硫是酸性气体,所以D中所盛药品是碱石灰或NaOH固体;
故答案为:三颈烧瓶;防倒吸;碱石灰;
(3)铜与浓硫酸在加热的条件下生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4═CuSO4+SO2↑+2H2O;
故答案为:Cu+2H2SO4═CuSO4+SO2↑+2H2O;
(4)从E处鼓入空气或氮气,使体系中的二氧化硫完全除净,所以操作为:打开旋塞E,从E管口向A中鼓入大量空气,故答案为:打开旋塞E,从E管口向A中鼓入大量空气;
(5)硫酸铜晶体溶于水溶液变蓝色;水加入浓硫酸中,放出大量热使液体飞溅;
故答案为:混合时放热,白色固体溶解,溶液变蓝色;水加入浓硫酸中,放出大量热使液体飞溅。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值,下列说法正确的是
A. 在标准状况下,4.48L水中含有的分子数目为0.2NA
B. 0.1mol![]() 离子含有的电子、中子数均为1.0NA
离子含有的电子、中子数均为1.0NA
C. 一定条件下,0.1mol![]() 与0.3mol
与0.3mol![]() 充分反应后的0.1NA个分子
充分反应后的0.1NA个分子
D. 总物质的量为0.1mol的CaO和![]() 混合物中,所含离子总数为0.2NA
混合物中,所含离子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物J是一种重要的有机中间体,可以由苯合成,具体合成路线如下:

(1)J的化学式为__________________ ;F的名称为__________________。
(2)B中官能团名称为____________________ 。
(3)I—J的反应类型为____________________ 。
(4)F -G的反应方程式为____________________ 。
(5)与I属于同种类型物质且苯环上有两个取代基的同分异构体有____种。符合下列条件的J的一种同分异构体结构简式为______。
①属于芳香族化合物 ②不能与金属钠反应 ③有3种不同化学环境的氢原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列几组物质中,互为同分异构体的有___________。
①O2和O3;②CH3CH2CH2CH(C2H5)CH3 和 CH3CH2CH(CH3)CH2C2H5;③丙烯和丁烯;④3-乙基己烷和辛烷;⑤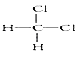 和
和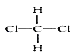
(2)用系统命名法给如图所示的有机物命名,其名称为_________________ 。
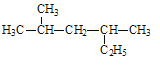
(3)甲烷在氯气中燃烧,可看到集气瓶内壁有黑色固体颗粒生成,瓶口产生大量白雾,据以上现象分析,上述反应的化学反应方程式为_______________________________。
(4)已知1g苯在氧气中完全燃烧放出的热量3.4 kJ,写出表示苯的燃烧热的热化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知在常温常压下:
①CH3OH(l)+ O2(g)=CO(g)+ 2H2O(g); ΔH=﹣355.0 kJ∕mol
②2CO(g)+ O2(g)= 2CO2(g) ΔH=-566.0 kJ/mol
③H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
写出表示甲醇燃烧热的热化学方程式:___________________________ 。
(2)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H=-49.0kJ/mol。相关数据如下:
CH3OH(g)+H2O(g) △H=-49.0kJ/mol。相关数据如下:
容器 | 甲 |
反应物投入量 | 1mol CO2(g)和3mol H2(g) |
平衡时c(CH3OH) | c1 |
平衡时能量变化 | 放出29.4kJ |
若甲中反应10s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是_____mol/(L·s)。
(3)铅蓄电池放电时总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。铅蓄电池放电时的正极反应式为____ ,当电路中有0.2mol电子转移时,理论上两电极质量变化的差为_______ g。
(4)甲烷可直接应用于燃料电池,该电池采用可传导O2-的固体氧化物为电解质,其工作原理如图所示:
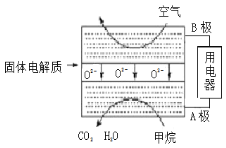
①A极电极反应式为____________________。
②若燃料电池消耗的空气在标准状况下的体积是5.6L(假设空气中O2体积为20%),则理论上消耗甲烷________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据各概念图作出的判断,正确的是
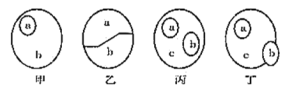
A. 在植物细胞内,甲图中a和b可以表示淀粉和葡萄糖的关系
B. 若乙中a和b分别代表DNA和RNA,则乙图可以代表病毒内的核酸
C. 丙图中a、b、c可分别表示磷脂、固醇和脂质之间的关系
D. 丁图a、b、c可分别表示蛋白质、激素和酶之间的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两同学欲制取纯净的Fe(OH)2 ,根据如图所示的装置进行试验。A管中是Fe+H2SO4 , B管中是NaOH溶液,请回答下列问题。
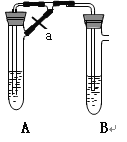
(1)同学甲:先夹紧止水夹a,使A管开始反应,在B管中观察到的现象是 。
(2)同学乙:打开a,使A管中反应一段时间再 夹紧止水夹a,实验中在B管中观察到的现象是 ,B中发生反应的离子方程式为
(3)同学乙打开a的目的 ; (填甲或乙)同学可成功。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Zn +2 HCl = ZnCl2 + H2↑的反应中,氧化剂是_________,失去电子的是_________,化合价降低的元素是_________,氧化产物是_________,还原产物是_________,画出该反应的双线桥并标出电子转移的方向和数目:__________________
Zn + 2 HCl = ZnCl2 + H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝石墨双离子电池是一种全新的低成本、高效能电池,反应原理为![]() ,电池结构如图所示。下列说法正确的是
,电池结构如图所示。下列说法正确的是

A. 放电时,外电路中电子向铝锂电极移动
B. 充电时,应将铝石墨电极与电源负极相连
C. 放电时,正极反应式为Cx(PF6) +e = xC + PF6
D. 充电时,若电路中转移1mol电子,则阴极质量增加9g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com