
【题目】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业作出了突出贡献。以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3+CO2+H2O===NH4HCO3;NH4HCO3+NaCl===NaHCO3↓+NH4Cl;2NaHCO3![]() Na2CO3+CO2↑+H2O。
Na2CO3+CO2↑+H2O。
【探究实例】
Ⅰ.原理分析 碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是________.
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,在溶液中首先结晶析出
Ⅱ.实验探究
(1)一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。

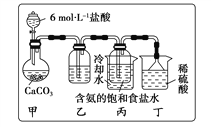
回答下列有关问题:
①丁装置中稀硫酸的作用是____________;
②实验结束后,分离出NaHCO3晶体的操作是________(填分离操作的名称)。如何进一步提纯(写出具体的操作)_________________________________________________。
(2)另一位同学用图中戊装置(其他装置未画出)进行实验。
①实验时,须先从_________管通入_______气体,再从_______管中通入_____________气体。
②有同学建议在戊装置的b导管下端连接己装置,理由是_______________。
【答案】 c 吸收未反应的NH3 过滤 向过滤器中加蒸馏水至完全淹没沉淀,静置,让水自然滤干,重复多次,直至滤液澄清。 a NH3 b CO2 增大CO2气体与溶液接触的面积,提高CO2在溶液中的吸收率
【解析】工业上侯氏制碱法是在饱和食盐水中通入氨气和二氧化碳,由于氨气在水中的溶解度大,所以先通入氨气,通入足量的氨气后再通入二氧化碳,生成了碳酸氢钠,由于碳酸氢钠的溶解度较小,所以溶液中有碳酸氢钠晶体析出,将碳酸氢钠晶体加热后得纯碱碳酸钠,
Ⅰ.a.碳酸氢钠易溶于水,选项a错误;b.碳酸氢钠受热易分解,与其在溶液中首先结晶析出无关,选项b错误;c.碳酸氢钠的溶解度相对于氯化铵来说碳酸氢钠的溶解度更小一些,所以在溶液中首先结晶析出,选项c正确;答案选c;
Ⅱ.(1)①.实验过程中氨气可能有剩余,而稀硫酸能与氨气反应,所以稀硫酸的作用是吸收末反应的NH3;②.分离出NaHCO3晶体的操作是分离固体与液体,常采用的实验操作是过滤操作;进一步提纯的操作为:向过滤器中加蒸馏水至完全淹没沉淀,静置,让水自然滤干,重复多次,直至滤液澄清;(2)a.制取碳酸氢钠时先要得到含氨的饱和食盐水,NH3极易溶于水,CO2能溶于水,所以应先从a管通入NH3,从而保证了从b管通入CO2时,CO2被充分反应;b.装置改动后反应物的CO2与溶液的接触面积变大,提高了CO2的吸收率,故答案为:增大CO2气体与溶液接触的面积,提高CO2在溶液中的吸收率。


科目:高中化学 来源: 题型:
【题目】A. B为短周期元素,两元素可形成化合物AB2,已知其原子序数分别为a和b,则a不可能为( )
A. b+4 B. b-5 C. b+6 D. b+8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的结构(键线式)及球棍模型如下:
该有机分子的核磁共振氢谱图如下(单位是ppm):
![]()
化学位移5
下列关于该有机物的叙述正确的是
A. 该有机物属于芳香族化合物
B. 键线式中的Et代表的基团为-CH3
C. 该有机物不同化学环境的氢原子有8种
D. 该有机物在氢氧化钠醇溶液加热的情况下能发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于取代反应的是
A. 甲烷与氯气反应生成一氯甲烷 B. 乙烯与水反应生成乙醇
C. 乙醇与氧气反应生成乙醛 D. 乙烯与高锰酸钾溶液反应生成CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体育竞技中服用兴奋剂既有失公平,也败坏了体育道德。某种兴奋剂的结构简式如图所示。有关该物质的说法中,正确的是

A. 1mol该物质分别与浓溴水和H2反应时分别最多消耗4mol和7mol
B. 滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
C. 该物质与苯酚属于同系物,遇溶液呈紫色
D. 该分子中的所有碳原子不可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之.”文中涉及的操作方法是( )
A. 蒸馏 B. 干馏 C. 升华 D. 萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。I可以用E和H在一定条件下合成:

已知以下信息:① A的核磁共振氢谱表明其只有一种化学环境的氢;
②R—CH=CH2![]() R—CH2CH2OH;③化合物F苯环上的一氯代物只有两种;④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
R—CH2CH2OH;③化合物F苯环上的一氯代物只有两种;④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
请回答下列问题:
(1)A的化学名称为______________。
(2)D的结构简式为_____________。
(3)E的分子式为_________________。
(4)F生成G的化学方程式为________________________,该反应类型为__________。
(5)I的结构筒式为____________。
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:
①苯环上只有两个取代基,②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,符合以上条件的同分异构体共有___________种。
J的一种同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道。请回答下列问题:
(1)R原子的基态电子排布式为___________________。
(2)X、Y原子的第一电离能大小顺序为______________。(用元素符号表示)
(3)X的常见单质分子结构中σ键数目为_____________。
(4)Z的最高价氧化物对应水化物的酸根离子空间构型为_____,中心原子的杂化轨道类型为________。
(5)某矿物晶体由Y、W、R三种元素组成,其晶胞结构如图所示。则该矿物的化学式为_________,若已知该晶胞的边长为a cm,则该晶胞的密度为_________g/cm3。(用含a、NA的代数式表示)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com