
【题目】物质Ⅲ(2,3—二氢苯并呋喃)是一种重要的精细化工原料,其合成的部分流程如下:

下列叙述正确的是
A. 可用溴水可以鉴别化合物Ⅰ和Ⅱ
B. 物质Ⅰ在NaOH醇溶液中加热可发生消去反应
C. 物质Ⅱ中所有原子可能位于同一平面内
D. 物质Ⅲ与足量H2加成所得产物分子中有2个手性碳原子
科目:高中化学 来源: 题型:
【题目】噻唑是一类含有N、S原子的具有芳香性的五元杂环化合物。已经在医药、农药、材料等领域显示出巨大的应用价值。噻唑类化合物的应用开发已经引起人们的广泛兴趣,并成为近年来研究的热点领域之一。某研究小组利用醋酸锰催化合成萘并噻唑衍生物G(2-邻氯苯甲酰氨基萘并[1,2-d]噻唑)的合成机理,合成路线如图:

已知:
![]()
![]() + H2O。
+ H2O。
根据以上信息,回答下列问题:
(1)写出有机物A的名称_____________。
(2)有机物C分子中所含的官能团为___________;由B生成C的化学方程式为____________。
(3)D与有机物E反应产物仅有F,则E的结构简式为__________,由D生成F的反应类型为__________。
(4)对目标产品G“2一邻氯苯甲酰氨基萘并[1,2一d]噻唑”的下列说法正确的是___________(填序号)
a.G的分子式为C18H10ON2SCl
b.F与G互为同分异构体
c.G可在一定条件下发生水解反应、加成反应等
d.G是一种难溶于水、易溶于有机溶剂的芳香族化合物
(5)邻氯苯甲酰氯的含有苯环的同分异构体共有_________种(不包括其自身),其中核磁共振氢谱(H-NMR)有3组峰的二氯苯甲醛分子的结构简式为:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组用如图所示装置验证卤素单质氧化性的相对强弱.下列说法不正确的是
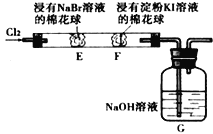
A. E处棉花球变成橙黄色,说明Cl2的氧化性比Br2强
B. F处棉花球变成蓝色,说明Br2的氧化性比I2强
C. E处发生反应的离子方程式为:Cl2 + 2Br- = 2Cl- + Br2
D. G装置中NaOH溶液与Cl2反应的离子方程式为:Cl2+2OH-=ClO-+Cl-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新泽茉莉醛是一种名贵的香料,合成过程中还能得到一种PC树脂,其合成路线如下:
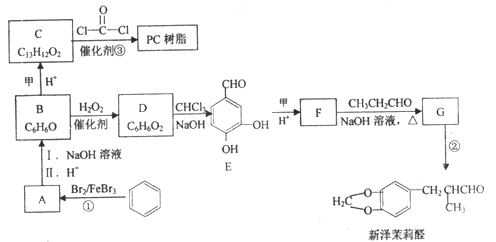
已知:
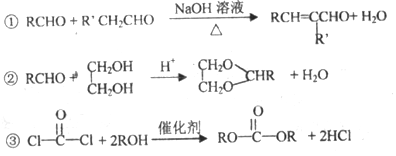
(1)写出反应①的化学方程式________________。
(2)写出符合下列条件并与化合物E互为同分异构体的有机物结构简式____________。
a. 能与浓溴水产生白色沉淀 b. 能与NaHCO3溶液反应产生气体
c. 苯环上一氯代物有两种
(3)反应②的反应类型是________。
(4)已知甲的相对分子质量为30,写出G的结构简式________________。
(5)已知化合物C的核磁共振氢谱有四种峰,写出反应③的化学方程式____________。
(6)结合已知①,以乙醇和苯甲醛为原料,选用必要的无机试剂合成 写出合成路线 __________________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
写出合成路线 __________________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2与漂粉精是常用的漂白剂。某兴趣小组对它们的漂白原理进行探究。过程如下:
I. 探究SO2的漂白性
实验一:将SO2分别通入0.1%品红水溶液和0.1%品红乙醇溶液中,观察到前者褪色而后者不褪色。
实验二:
| 试管中的液体 | 现象 |
a. 0.1 mol/L SO2溶液(pH=2) | 溶液逐渐变浅,约90s后完全褪色 | |
b. 0.1 mol/L NaHS03溶液(pH=5) | 溶液立即变浅,约15s后完全褪色 | |
c. 0.1 mol/L Na2SO3溶液( pH=10) | 溶液立即褪色 | |
d. pH=10NaOH溶液 | 红色溶液不变色 | |
e. pH=2H2SO4溶液 | 红色溶液不变色 |
(1)实验d的目的是____________。
(2)由实验一、二可知:该实验条件下,SO2使品红溶液褪色时起主要作用的微粒是____________。
(3)已知S02使品红溶液褪色过程是可逆的。兴趣小组继续试验:向a实验后的无色溶液中滴入Ba(OH)2溶液至pH=10时,生成白色沉淀,溶液变红。
请用离子方程式和必要的文字说明出现上述现象的原因____________。
II. 探究SO2与漂粉精的反应
实验三:
操作 | 现象 |
| i. 液面上方出现白雾; ii. 稍后,出现浑浊,溶液变为黄绿色; iii. 稍后,产生大量白色沉淀,黄绿色褪去 |
小组同学对上述现象进行探究:
(1)向水中持续通入SO2,未观察到白雾。推测现象i的白雾由HCl小液滴形成,进行如下实验:
a. 用湿润的碘化钾淀粉试纸检验白雾,无变化;
b. 用酸化的AgNO3溶液检验白雾,产生白色沉淀。
①实验a目的是____________________。
②由实验a、b不能判断白雾中含有HCl,理由是____________。
(2)现象ii中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应。通过进一步实验确认了这种可能性,其实验方案是____________。
(3)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀x中加入稀HCl,无明显变化。取上层清液,加入BaCl2溶液,产生白色沉淀。则沉淀X中含有的物质是____________。
②用离子方程式解释现象iii中黄绿色褪去的原因________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应在体积为5L的恒容密闭容器中进行,在0~3分钟内各物质的量的变化情况如图所示(A,B,C均为气体,且A气体有颜色)。
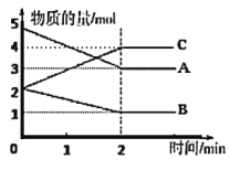
(1)该反应的化学方程式为______________________________;
(2)反应开始至2分钟时,A的平均反应速率为______________;
(3)下列措施能使该反应加快的是____________(仅改变一个条件)
a.降低温度 b.缩小容积 c.恒容时充入Ar气,增大压强
(4)能说明该反应已达到平衡状态的是__________(填序号)。
①单位时间内生成nmolB的同时生成2nmolC
②单位时间内生成nmolB的同时生成2nmolA
③容器内压强不再随时间而发生变化的状态
④A、B、C的物质的量浓度之比保持3:1:4不变的状态
⑤混合气体的颜色不再改变的状态
⑥混合气体的密度不再改变的状态
⑦υ逆(B)=2υ正(C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电子式的相关描述中正确的是( )
A. CCl4的电子式为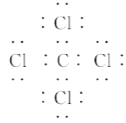
B. CaCl2的电子式
C. 由氨气的电子式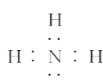 可知,每个氨气分子含有8个电子
可知,每个氨气分子含有8个电子
D. 用电子式表示氯化氢的形成过程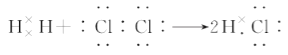
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是

A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH3是形成无机颗粒物的催化剂
D. 雾霾的形成与过度施用氮肥有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10 mol·L-1CH3COOH
溶液和HCN溶液所得滴定曲线如右图。下列说法正确的是

A. 点①和点②所示溶液中:c(CH3COO-)<c(CN-)
B. 点③和点④所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C. 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
D. 点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com