
【题目】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g) 达到平衡。下列说法正确的是
CH3OH(g) 达到平衡。下列说法正确的是
容器 | 温度/K | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | ||
c(H+) | c(CO) | c(CH3OH) | c(CH3OH) | ||
Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
Ⅱ | 400 | 0.40 | 0.20 | 0 | |
Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
A. 该反应的逆反应放热
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C. 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
【答案】D
【解析】
A、分析Ⅰ、Ⅲ中数据知反应开始时Ⅰ中加入的H2、CO与Ⅲ中加入甲醇的物质的量相当,平衡时甲醇的浓度:Ⅰ>Ⅲ,温度:Ⅰ<Ⅲ,即升高温度平衡逆向移动,该反应的逆反应放热反应,选项A错误;B、Ⅱ相当于将容器Ⅰ的体积缩小二分之一,该反应正向为气体物质的量减小的反应,增大压强平衡正向移动,达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的小,选项B错误;C、Ⅰ和Ⅱ对比,Ⅱ相当于将容器Ⅰ的体积缩小二分之一,该反应正向为气体物质的量减小的反应,增大压强平衡正向移动,则Ⅱ中氢气的浓度小于Ⅰ中氢气浓度的2倍,Ⅲ和Ⅰ对比,平衡逆向移动,氢气浓度增大,故达到平衡时,容器Ⅱ中c(H2)小于容器Ⅲ中c(H2)的两倍,选项C错误;D、温度:Ⅲ>Ⅰ,当其他条件不变时,升高温度反应速率加快,故达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大,选项D正确。答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列各组粒子,互为同位素的是_____(填编号,下同),互为同素异形体的是_______,互为同分异构体的是__________,属于同一种物质的是___________。
① 16O2和18O3 ②质子数相同而中子数不同的两种粒子
③H D T ④ ⑤正丁烷和异丁烷
⑤正丁烷和异丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某药物H的合成路线如下:
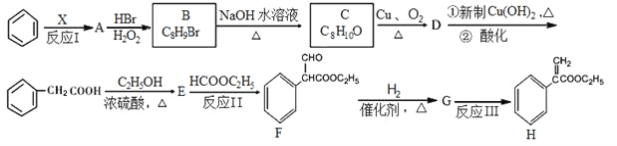
试回答下列问题:
(1)反应Ⅰ所涉及的物质均为烃,氢的质量分数均相同,则X的结构式为__________,A的名称为___________。
(2)反应Ⅱ的反应类型是________________。
(3)B的结构简式是____________;E的分子式为___________;F中含氧官能团的名称是_________。
(4)由C→D反应的化学方程式为______________。由G→H反应的化学方程式为_____________。
(5)化合物G酸性条件下水解产物之一M有多种异构体,满足下列条件的结构有_______种。
①能发生水解反应和银镜反应;②能与FeCl3发生显色反应;③苯环上只有两个取代基。
(6)参照上述合成路线,设计一条由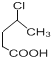 制备
制备![]() 的合成路线流程__________________。
的合成路线流程__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于淀粉和纤维素的叙述中,不正确的是( )
A.它们都是混合物
B.它们互为同分异构体
C.它们都能水解生成葡萄糖
D.它们都是天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸香叶酯是一种食品香料,可以由香叶醇与甲酸发生酯化反应制得。

下列说法正确的是
A. 香叶醇的分子式为C11H18O
B. 香叶醇在浓硫酸、加热条件下可发生消去反应
C. l mol甲酸香叶酯可以与2 molH2发生加成反应
D. 香叶醇与甲酸香叶酯均不能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤粉隔绝空气加强热,除主要得到焦炭外,还能得到下表所列的物质:
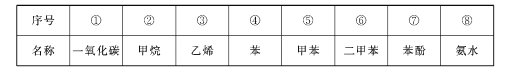
回答下列问题:
(1)天然气的主要成分是____(填序号);
(2)滴加氯化铁溶液能变为紫色的是____(填序号);
(3)可用于生产制尼龙的原料环己烷的是____(填序号);
(4)能发生加聚反应,生成物可用来制造食品包装袋的是____(填序号);
(5)甲苯的一氯取代产物有___种;
(6)二甲苯的三种同分异构体中,沸点最低的是_____(填结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)L的元素符号为________ ;M在元素周期表中的位置为________________;五种元素的原子半径从大到小的顺序是_________________(用元素符号表示)。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B ,A的沸点比同主族其他气态氢化物___________(填“高”或“低”),原因是________________________________,B中存在的化学键类型为____________。
A极性共价键 B非极性共价键 C 离子键
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为__________,其最高价氧化物对应的水化物化学式为__________。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。
a +99.7 kJ·mol-1 b +29.7 kJ·mol-1 c -20.6 kJ·mol-1 d -241.8 kJ·mol-1

(4)Y、硅与硫三种元素非金属性由强到弱的顺序为________________(用元素符号表示)。某同学用如图所示装置验证Y、硅与硫三种元素非金属性强弱(夹持仪器已略去,气密性已检验)。Ⅰ、Ⅱ、Ⅲ所加入的试剂分别为:_________________________(用化学式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com