
| A. | H+、Fe2+、NO3-、SO42- | B. | Na+、H+、AlO2-、HCO3- | ||
| C. | Ca2+、Fe3+、CO32-、CH3COO- | D. | Ca2+、Na+、HCO3-、Cl- |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应,不能相互促进水解等,则离子大量共存,以此来解答.
解答 解:A.H+、Fe2+、NO3-发生氧化还原反应,不能大量共存,故A错误;
B.H+、AlO2-结合生成沉淀,H+、HCO3-结合生成水和气体,AlO2-促进HCO3-的电离,不能大量共存,故B错误;
C.Fe3+分别与CO32-、CH3COO-相互促进水解,Ca2+、CO32-结合生成沉淀,不能大量共存,故C错误;
D.该组离子之间不反应,可大量共存,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重氧化还原反应、水解反应及复分解反应的离子共存考查,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 16 | B. | 17 | C. | 18 | D. | 19 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | K+、CO32-、Cl-、NO3- | B. | K+、Fe2+、I-、SO42- | ||
| C. | Ba2+、Na+、Cl-、NO3- | D. | Na+、Ca2+、Al3+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2NaHCO3═Na2CO3+CO2↑+H2O | B. | MnO2+4 HCl(浓)═MnCl2+Cl2↑+2 H2O | ||
| C. | 2 H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2 H2O+O2↑ | D. | Na2CO3+CaCl2═CaCO3↓+2NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
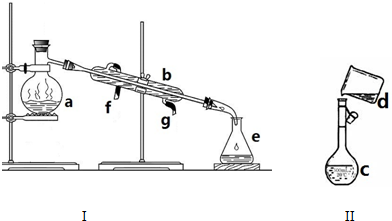
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
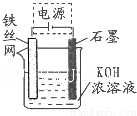 铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
铁及其化合物在生产、生活中有广泛应用.请回答下列问题:| 温度/℃ | 1000 | 1115 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com