
×å ÖÜĘŚ | ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A |
| 2 | Li | Be | B | C | N | O | F |
| 3 | Na | Mg | Al | Si | P | S | Cl |
 £®
£® £®
£®·ÖĪö £Ø1£©Al3+µÄÖŹ×ÓŹżĪŖ13£¬ŗĖĶāµē×ÓŹżĪŖ10£»
£Ø2£©Ö»ŗ¬C”¢OÖ®¼äµÄ¹²¼Ū¼ü£¬CÓėOÖ®¼ä“ęŌŚĮ½¶Ō¹²ÓƵē×Ó¶Ō£»
£Ø3£©Ķ¬ÖÜĘŚ“Ó×óĻņÓŅ½šŹōŠŌ¼õČõ£¬Ķ¬Ö÷×å“ÓÉĻµ½ĻĀ½šŹōŠŌŌöĒ棻µē×Ó²ćŌ½¶ą£¬Ō×Ó°ė¾¶Ō½“ó£¬Ķ¬ÖÜĘŚ“Ó×óĻņÓŅŌ×Ó°ė¾¶¼õŠ”£»
£Ø4£©·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦Ēā»ÆĪļĪČ¶ØŠŌŌ½Ē棬¶ŌÓ¦×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌŌ½Ē棻
£Ø5£©Na”¢Al×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļÖ®¼ä·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£®
½ā“š ½ā£ŗ£Ø1£©Al3+µÄÖŹ×ÓŹżĪŖ13£¬ŗĖĶāµē×ÓŹżĪŖ10£¬Al3+µÄ½į¹¹Ź¾ŅāĶ¼ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø2£©CO2ÖŠÖ»ŗ¬C”¢OÖ®¼äµÄ¹²¼Ū¼ü£¬CÓėOÖ®¼ä“ęŌŚĮ½¶Ō¹²ÓƵē×Ó¶Ō£¬µē×ÓŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ¹²¼Ū¼ü£» £»
£»
£Ø3£©ÉĻŹöŌŖĖŲÖŠ£¬½šŹōŠŌ×īĒæµÄŌŖĖŲŹĒNa£¬Ō×Ó°ė¾¶×īŠ”µÄŌŖĖŲŹĒF£¬¹Ź“š°øĪŖ£ŗNa£»F£»
£Ø4£©F”¢Cl”¢SµÄĒā»ÆĪļÖŠĪČ¶ØŠŌ×īČõµÄŹĒH2S£¬N”¢P”¢SiµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļÖŠĖįŠŌ×īĒæµÄŹĒHNO3£¬
¹Ź“š°øĪŖ£ŗH2S£»HNO3£»
£Ø5£©Na”¢Al×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļÖ®¼ä·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒNaOH+Al£ØOH£©3=NaAlO2+2H2O£¬
¹Ź“š°øĪŖ£ŗNaOH+Al£ØOH£©3=NaAlO2+2H2O£®
µćĘĄ ±¾Ģāæ¼²éĪ»ÖĆ”¢½į¹¹”¢ŠŌÖŹµÄÓ¦ÓĆ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŌŖĖŲÖÜĘŚĀÉ”¢ŌŖĖŲ»ÆŗĻĪļĪŖ½ā“šµÄ¹Ų¼ü£¬×¢Ņā¹ęĀÉŠŌÖŖŹ¶µÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
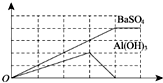 ŅŃÖŖĻņČÜŅŗQÖŠµĪ¼ÓČÜŅŗPæÉÉś³ÉĮ½ÖÖ³Įµķ£¬ĖłµĆ³ĮµķĮæÓėĖł¼ÓČėµÄPČÜŅŗµÄĢå»ż¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņQ”¢P·Ö±šĪŖ£Ø””””£©
ŅŃÖŖĻņČÜŅŗQÖŠµĪ¼ÓČÜŅŗPæÉÉś³ÉĮ½ÖÖ³Įµķ£¬ĖłµĆ³ĮµķĮæÓėĖł¼ÓČėµÄPČÜŅŗµÄĢå»ż¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņQ”¢P·Ö±šĪŖ£Ø””””£©| A£® | QĪŖNH4Al£ØSO4£©2£¬PĪŖBa£ØOH£©2 | B£® | QĪŖBa£ØOH£©2£¬PĪŖĆ÷·Æ | ||
| C£® | QĪŖĆ÷·Æ£¬PĪŖBa£ØOH£©2 | D£® | QĪŖBa£ØAlO2£©2£¬PĪŖĮņĖįĀĮ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
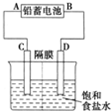 ČēĶ¼ŹĒŅŌĒ¦Šīµē³ŲĪŖµēŌ“£¬Ä£ÄāĀČ¼ī¹¤Ņµµē½ā±„ŗĶŹ³ŃĪĖ®µÄ×°ÖĆĶ¼£ØC”¢D¾łĪŖŹÆÄ«µē¼«£©£®
ČēĶ¼ŹĒŅŌĒ¦Šīµē³ŲĪŖµēŌ“£¬Ä£ÄāĀČ¼ī¹¤Ņµµē½ā±„ŗĶŹ³ŃĪĖ®µÄ×°ÖĆĶ¼£ØC”¢D¾łĪŖŹÆÄ«µē¼«£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²śÉś»ĘĀĢÉ«µÄĘųĢå | B£® | ²śÉś°×ŃĢ | ||
| C£® | ²śÉś°×Īķ | D£® | ƻӊĆ÷ĻŌĻÖĻó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | øÖ°åŹĒÕż¼«£¬Õż¼«ÉĻ·¢Éś»¹Ō·“Ó¦ | |
| B£® | ·ÅµēŹ±µē×ÓµÄĮ÷Ļņ£ŗÕż¼«”śµ¼Ļß”śøŗ¼« | |
| C£® | ·ÅµēŹ±OH-ĻņÕż¼«ŅĘ¶Æ | |
| D£® | ·ÅµēŹ±×Ü·“Ó¦ĪŖ£ŗ4Li+2H2O+O2=4LiOH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅČ© | B£® | ¼×Č© | C£® | ±ūČ© | D£® | ¶”Č© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2KOH£Øaq£©+H2SO4£Øaq£©=K2SO4£Øaq£©+2H2O £Øl£©£»”÷H=-114.6kJ/mol | |
| B£® | KOH£Øs£©+$\frac{1}{2}$H2SO4£Øaq£©=$\frac{1}{2}$K2SO4£Øaq£©+H2O £Øl£©£»”÷H=-57.3 kJ/mol | |
| C£® | 2KOH£Øs£©+H2SO4£Øaq£©=K2SO4£Øaq£©+2H2O £Øl£©£»”÷H=-114.6 kJ/mol | |
| D£® | KOH£Øaq£©+$\frac{1}{2}$ H2SO4£Øaq£©=$\frac{1}{2}$K2SO4£Øaq£©+H2O £Øl£©£»”÷H=-57.3kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1£ŗ1 | B£® | 3£ŗ4 | C£® | 9£ŗ8 | D£® | 4£ŗ3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com