
【题目】NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.在0.1mol·L-1的Na2CO3溶液中,阴离子总数一定大于0.1NA
B.常温常压下,由32gO2与O3组成的混合气体中含有的分子总数小于NA
C.36.0gCaO2与足量水完全反应,转移的电子数为NA
D.1molCH4与1molCl2混合,充分反应后,生成气体分子数为NA
【答案】B
【解析】
A.0.1mol·L-1的Na2CO3溶液体积未知,无法确定溶液中阴离子总数是否大于0.1NA,故A错误;
B.32gO2的物质的量为![]() =1mol,O2分子数目为NA,而含有O3相同质量的O3所含分子数小于NA,则组成的混合气体中含有的分子总数小于NA,故B正确;
=1mol,O2分子数目为NA,而含有O3相同质量的O3所含分子数小于NA,则组成的混合气体中含有的分子总数小于NA,故B正确;
C.36.0gCaO2的物质的量为![]() =0.5mol,与足量水完全反应生成氢氧化钙和氧气,CaO2与水的反应为歧化反应,氧元素由-1价变为0价和-2价,则0.5mol CaO2转移的电子数为0.5mol ×1×NA=0.5 NA,故C错误;
=0.5mol,与足量水完全反应生成氢氧化钙和氧气,CaO2与水的反应为歧化反应,氧元素由-1价变为0价和-2价,则0.5mol CaO2转移的电子数为0.5mol ×1×NA=0.5 NA,故C错误;
D.将1molCH4与1molCl2混合,充分反应后,生成一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷和氯化氢,其中氯化氢与一氯甲烷为气体,根据元素守恒可知,氯化氢的物质的量为1mol,则气体分子数大于NA,故D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】某兴趣小组用合金铝、铁、铜的废弃合金为原料制取硝酸铜晶体和氢氧化铝并测定氢氧化铝的纯度,设计的主要流程如下:

已知:Fe2+沉淀的pH范围为7.0~9.0;Fe3+沉淀的pH范围为1.9~3.2;Cu2+沉淀的pH范围为4.7~6.7。
(1)写出合金中加入NaOH溶液后所发生的离子反应方程式___,试剂X的名称为__。
(2)加入Z的作用是调节溶液的pH,pH范围应为___;下列可作为试剂z的是___。
a.铜粉 b.氨水 c.氧化铜 d.硫酸铜
(3)实验操作①依次是____、___,过滤洗涤即可得到硝酸铜晶体。
(4)根据流程图内数据计算:滤渣C中氢氧化铝的质量分数为___。(用m、n的代数式表示)
(5)按该流程的操作步骤,氢氧化铝质量分数的测定结果可能性是非常大的,原因有①___;②____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL某浓度的稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,体积已换算成标准状态):
时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL) | 0 | 50 | 120 | 232 | 290 | 310 |
(1)2~3min段的反应速率比1~2min段的反应速率__________(填“块”或“慢”),原因是______;
(2)求2~3min段以HCl的浓度变化来表示的平均反应速率(设溶液体积不变)____________;
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液,你认为可行的是(填编号)____________。
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿托酸是一种常用的医药中间体,其结构如图所示,下列有关说法正确的是( )
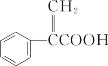
A.阿托酸的分子式为C9H6O2
B.阿托酸分子中所有原子可能处于同一平面
C.在一定条件下,1mol阿托酸最多能和5molH2发生反应
D.阿托酸能发生取代、加成、水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用如图所示的装置及药品进行酸性强弱比较的实验。下列说法正确的是

A.①和②中发生的反应均为置换反应
B.其他条件不变,可用盐酸替代稀硫酸
C.一段时间后,②中有胶冻状物质生成
D.该实验证明酸性:硫酸>硅酸>碳酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.1000mol·L-1的盐酸分别滴定20.00mL 0.1000mol·L-1氨水和20.00mL 0.1000mol·L-1 NaOH溶液,滴定曲线如图所示。下列说法不正确的是
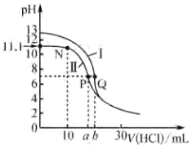
A.25℃,Kb(NH3·H2O)的数量级为10-5
B.N点处的溶液中:c(NH![]() )>c(NH3·H2O)
)>c(NH3·H2O)
C.曲线II滴定终点时所选的指示剂为酚酞
D.Q点所加盐酸的体积为b mL,则b=20
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaS在环境保护、制备电致发光材料等方面用途非常广泛。回答下列问题:
(1)制取CaS的反应如下:
反应(I):CaSO4(s)+2C(s)![]() CaS(s)+2CO2(g) △H1
CaS(s)+2CO2(g) △H1
反应(II):CaCO3(s)+H2S(g)![]() CaS(s)+H2O(g)+CO2(g) △H2=+165kJ·mol-1
CaS(s)+H2O(g)+CO2(g) △H2=+165kJ·mol-1
①若在恒温恒容密闭容器中只发生反应(I),达到平衡时向容器中通入少量CO2,则反应再次达到平衡时c(CO2)将___(填“增大”“减小”或“不变”)。
②已知下列热化学方程式:.
i:S2(g)+CaSO4(s)![]() CaS(g)+2SO2(g) △H=+240.4kJ·mol-1
CaS(g)+2SO2(g) △H=+240.4kJ·mol-1
ii:2SO2(g)+4CO(g)=S2(g)+4CO2(g) △H=+16.0kJ·mol-1
iii:C(s)+CO2(g)=2CO(g) △H=+172.5kJ·mol-1
则反应(I)的△H1=___kJ·mol-1。
③反应(II)的△S___(填“>”“<”或“=”)0。若反应(II)在恒温恒容密闭容器中进行,能说明该反应已达到平衡状态的是___(填字母)。
A.v(H2O)正=v(CO2)正
B.容器中气体总压强不再随时间变化
C.容器中同时存在H2S(g)、CO2(g)和H2O(g)
D.单位时间内断裂H-S键与断裂C=O键数目相等
(2)CaS能被许多物质氧化,有关反应的lgKp与温度关系如图(Kp为以分压表示的平衡常数;分压=总压×物质的量分数;图中数据由压强单位为kPa得出)。
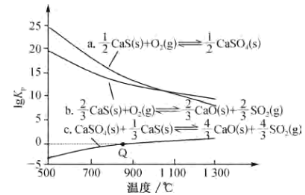
①属于吸热反应的是___ (填“a”“b”或“c”)。
②相同温度下,反应a、b、c的lgKp(a)、lgKp(b)、lgKp(c)之间满足的关系是lgKp(c)=___。
③反应c在Q点时:p(SO2)=___kPa,以浓度表示的平衡常数Kc=___Kp[用R、T表示;已知气体的压强、体积、温度满足pV=nRT(n为气体的物质的量,R为恒量)]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,向20mL0.1mol·L-1MOH溶液中滴加0.1mol·L-1CH3COOH溶液,所得溶液的pH及导电能力变化如图所示。下列叙述正确的是( )
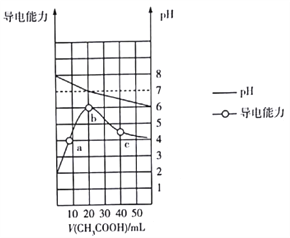
A. MOH是强电解质 B. b点对应的盐不水解
C. 水的离子积Kw:b>c>a D. c点溶液中c(CH3COO-)>c(M+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为________。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为
NO+NO2+2OH![]() 2
2![]() +H2O
+H2O
2NO2+2OH![]()
![]() +
+![]() +H2O
+H2O
①下列措施能提高尾气中NO和NO2去除率的有________(填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是________(填化学式);吸收后排放的尾气中含量较高的氮氧化物是________(填化学式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为![]() 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性NaClO溶液中,HClO氧化NO生成Cl和![]() ,其离子方程式为________。
,其离子方程式为________。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com