
从海水中可以获得淡水、食盐,也可提取镁和溴等物质。
(1)海水淡化的方法主要有______ (填一种)。
(2)从海水中提取镁的流程如下图所示:

流程中分离Mg(OH)2沉淀的方法是_____________________;
写出反应②的化学方程式____________________________。
(3)从海水中提取溴的主要反应原理是向浓缩的海水中通入氯气,将溴离子氧化。试写出该反应的离子方程式________________________________________________。
科目:高中化学 来源:2014-2015学年湖南省五市十校教研教改共同体高三第一次联考化学试卷(解析版) 题型:选择题
类推的思维方法在化学学习与研究中经常用到,但有时会产生错误的结论。因此,推出的结论最终要经过实践的检验才能决定其是否正确。以下几种类推结论中,正确的是
A.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3
B.IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3
C.Fe3O4可以写成FeO·Fe2O3;Pb3O4也可以写成PbO·Pb2O3
D.NaHSO4与NaHSO3溶于水显酸性,由所有酸式盐溶于水显酸性
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省扬州市高二上学期期末考试化学试卷(解析版) 题型:选择题
玻璃器皿上沾有一些用水洗不掉的残留物,其洗涤方法正确的是
①用酒精洗涤试管内壁上残留的碘②用酒精洗涤试剂瓶中残留的苯酚③用稀氨水洗涤试管壁上银镜④用热碱液洗涤试管内壁上的油脂
A.①③④ B.②③④ C.①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省益阳市高二1月月考化学试卷(解析版) 题型:选择题
在密闭容器中进行如下反应:X2(g)+Y2(g)  2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
A.Z为0.3mol/L B.Y2为0.4mol/L
C.X2为0.2mol/L D.Z为0.4mol/L
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省益阳市高二1月月考化学试卷(解析版) 题型:选择题
用水稀释0.1mol/L的CH3COOH溶液,其中随水的量增大的有
(1)n(H+) (2)c(H+) (3)c(H+)/c(CH3COOH) (4)c(CH3COOH)/ c(H+)
A.(1)(3) B.(1)(4) C.(3)(4) D.(1)(2)
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省怀化市高一上学期期末化学试卷(解析版) 题型:填空题
将1.0 mol X气体和1.0 mol Y气体混合于2 L的密闭容器中,发生反应2X(g)+Y(g) 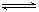 2Z(g)+2W(g),2min末,测得生成了0.4 mol W。
2Z(g)+2W(g),2min末,测得生成了0.4 mol W。
(1)前2min以X表示的平均反应速率为 ;
(2)下列叙述能说明该反应已达到化学平衡状态的是 。
A.单位时间里,消耗2 mol X,同时生成2 mol W
B.单位时间里,消耗2 mol X,同时也消耗了2 mol Z
C.反应混合物中各物质的浓度相等
D.反应混合物中各物质的浓度不再改变
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省怀化市高一上学期期末化学试卷(解析版) 题型:选择题
把镁条投入到盛有盐酸的敞口容器中,下列因素对产生H2速率没有影响的是
A.Cl-的浓度 B.镁条的表面积 C.溶液的温度 D.H+的浓度
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省绥化市三校高二上学期期末联考化学试卷(解析版) 题型:填空题
(10分)如图所示,用甲醇和氧气以及强碱做电解质溶液的新型燃料电池做电源,对A、B 装置通电一段时间后,发现有1.6g甲醇参加反应且③电极增重(假设工作时无能量损失)。
请回答下列问题:

(1)分别指出F电极、②电极的名称 、 。
(2)④电极的反应式: 。
E电极的反应式: 。
(3)若A池中原混合液的体积为500 mL,CuSO4、K2SO4浓度均为0.1 mol/L,电解过程中A池中共收集到标准状况下的气体 L,①、③电极析出固体物质的量之比 。
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省等校高一上学期期中联考化学试卷(解析版) 题型:选择题
某元素R的阴离子R 2–核外共有a个电子,核内有b个中子,则表示R原子的符号正确的是
A. B.
B. C.
C. D.
D.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com