
| A������ˮ�ĵ���̶���С������ˮ�ĵ���̶���� |
| B�����ڡ��ۻ�ϣ�����pH=7����������Һ��������ڣ��� |
| C�����١��ܻ�ϣ�����c(CH3COO��)��c(H��)������Һһ���ʼ��� |
| D�����ķ���Һ�ֱ�ϡ��100������Һ��pH���ۣ��ܣ��٣��� |
 H++OH�������������ᣬ������ǿ�ᣬ�١��ڣ���������������Ũ�ȣ�ʹ����ƽ�����ƣ�ˮ�ĵ���̶ȼ�С�������ˮ�ĵ���̶ȴ��ڢڣ����ۡ��ܣ�������������������Ũ����ȣ������ˮ�ĵ���̶������ͬ��Ҳ�������ͬ����A���ڢ۵�������ʱ��ǿ��������������С���������������������ӣ�����������Һ�ʼ��Ի�pH>7���������ҺpH=7����������Һ�����ҪС��ǿ����Һ����B��ȷ�����������ᣬ���ڵ���ƽ�⣺CH3COOH
H++OH�������������ᣬ������ǿ�ᣬ�١��ڣ���������������Ũ�ȣ�ʹ����ƽ�����ƣ�ˮ�ĵ���̶ȼ�С�������ˮ�ĵ���̶ȴ��ڢڣ����ۡ��ܣ�������������������Ũ����ȣ������ˮ�ĵ���̶������ͬ��Ҳ�������ͬ����A���ڢ۵�������ʱ��ǿ��������������С���������������������ӣ�����������Һ�ʼ��Ի�pH>7���������ҺpH=7����������Һ�����ҪС��ǿ����Һ����B��ȷ�����������ᣬ���ڵ���ƽ�⣺CH3COOH H++CH3COO����NaOH�����������ӣ���С������Ũ�ȣ��ٽ�����������������ӣ���٢ܻ��Һ�ʼ��ԡ����ԡ���������ʱ�������ܴ���c(CH3COO��)��c(H��)����C����ϡ��100����ǿ���ǿ���ǿ�������Һ�������ӻ�����������Ũ�ȱ仯�ϴ���ҺpH�仯�ϴ���Ϊϡ���ܴٽ����������ĵ��룬�����������Һ�������ӻ�������������Ũ�ȱ仯��С����ҺpH�仯��С�����ϡ����ҺpH����>��>��>�ڣ���D��ȷ��
H++CH3COO����NaOH�����������ӣ���С������Ũ�ȣ��ٽ�����������������ӣ���٢ܻ��Һ�ʼ��ԡ����ԡ���������ʱ�������ܴ���c(CH3COO��)��c(H��)����C����ϡ��100����ǿ���ǿ���ǿ�������Һ�������ӻ�����������Ũ�ȱ仯�ϴ���ҺpH�仯�ϴ���Ϊϡ���ܴٽ����������ĵ��룬�����������Һ�������ӻ�������������Ũ�ȱ仯��С����ҺpH�仯��С�����ϡ����ҺpH����>��>��>�ڣ���D��ȷ��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��CH3OH(l) +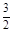 O2(g)=CO2(g)+2H2O(l)��H����725.8 kJ��mol-1 O2(g)=CO2(g)+2H2O(l)��H����725.8 kJ��mol-1 |
| B��2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)��H����1452 kJ��mol-1 |
C��CH3OH(l) +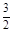 O2(g)=CO2+2H2O��H����725.8 kJ��mol-1 O2(g)=CO2+2H2O��H����725.8 kJ��mol-1 |
D��CH3OH(l) +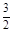 O2(g)=CO2(g)+2H2O(l)��H����725.8 kJ��mol-1 O2(g)=CO2(g)+2H2O(l)��H����725.8 kJ��mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 L
L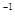 �Ĵ�����Һ����μ�������ʵ���Ũ�ȵ��ռ���Һ���ⶨ�����Һ���¶ȱ仯��ͼ��ʾ�����й��ڻ����Һ�����˵���������
�Ĵ�����Һ����μ�������ʵ���Ũ�ȵ��ռ���Һ���ⶨ�����Һ���¶ȱ仯��ͼ��ʾ�����й��ڻ����Һ�����˵���������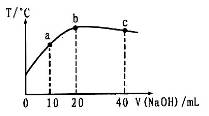
| A������ĵ���ƽ�ⳣ����b�㣾a�� |
| B����ˮ�������c(OH��)��b�㣾a�� |
| C����a�㵽b�㣬�����Һ�п��ܴ��ڣ�c(Na��)��c(CH3COO��) |
| D��b�㵽c�㣬�����Һ��һֱ���ڣ�c(Na��)��c(CH3COO��)��c(OH��)��c(H+) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.1 mol��L��1������Һ�У�c(H+)= c(CH3COO��)+c(OH��) |
| B���к�pH���������ͬ������ʹ��ᣬ����NaOH�������ߴ���ǰ�� |
| C��ͬ��ͬŨ�ȵ�NaOH�ͳ���ʯ��ˮ�У�ˮ�ĵ���̶���ͬ |
| D��NaHCO3��Һ�У�c(Na+)��c(HCO3��)��c(H2CO3)��c(OH��)��c(H+) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������c1mol/L�Ĵ����ϡ10��������pH����1 |
| B������c2 mol/L������������Һ��ϡ10��������pH��С1 |
| C����c1? V1=c2?V2������Һ��c(CH3COO��)=c(Na+) |
| D�������Һ��pH=7������Һ��c(CH3COO��)=c(Na+) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ��� | �� | �� |
| pH | 12 | 2 |
| ��Һ | ����������Һ | ������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.1 mol | B��0.15 mol | C��0.25 mol | D��0.35 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���������� | B����Ӧ����Һc(A-)=c(M+) |
| C�����ɵ��β�ˮ�� | D�����������ʵ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com